
【题目】乙二醇(沸点:197.3℃)是一种重要的基础化工原料。由煤基合成气(主要成分CO、H2)与氧气先制备得到草酸二甲酯(沸点:164.5℃),再加氢间接合成乙二醇,具有反应条件温和、环境污染小等优点。反应过程如下:
反应I:4NO(g)+4CH3OH(g)+O2(g)![]() 4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
反应II:2CO(g)+2CH3ONO(g)![]() CH3OOCCOOCH3(l)+2NO(g) △H2=b kJ·mol-1
CH3OOCCOOCH3(l)+2NO(g) △H2=b kJ·mol-1
反应III:CH3OOCCOOCH3(1)+4H2(g)![]() HOCH2CH2OH(1)+2CH3OH(g)△H3 =c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g)△H3 =c kJ·mol-1
请回答下列问题:
(1)煤基合成气间接合成乙二醇的总热化学方程式是_____________________________,已知该反应在较低温条件下能自发进行。说明该反应的△H ______0(填“>”“<”或“=”)。
(2)CO、CH3ONO各0.4mol在恒温、容积恒定为2L的密闭容器中发生反应II,达到平衡时CO的体积分数与NO的体积分数相等,计算该反应的化学平衡常数K=_____________。若此时向容器中再通入0.4molNO,一段时间后,达到新平衡时NO的体积分数与原平衡时相比______(填“增大”“相等”“减小”或“不能确定”)。
(3)温度改变对反应II的催化剂活性有影响,评价催化剂的活性参数——空时收率和CO的选择性可表示如下:
空时收率=CH3OOCCOOCH3质量/反应时间×催化剂的体积
CO的选择性=合成[CH3OOCCOOCH3所消耗的CO的物质的量/反应掉的CO的物质的量]×100%
在不同温度下,某学习小组对四组其他条件都相同的反应物进行研究,经过相同时间th,测得空时收率、CO的选择性数据如下表所示。
反应温度(℃) | 空时收率(g·mL-1·h-1) | CO的选择性(%) |
130 | 0.70 | ①72.5 |
140 | 0.75 | ②71.0 |
150 | 0.71 | ③55.6 |
160 | 0.66 | ④63.3 |
下列说法正确的是________(填字母代号)。
A.温度升高,空时收率先增大后减小,说明△H2>0
B.温度升高,催化剂活性逐渐减弱,对CO的选择性逐渐降低
C.综合考虑空时收率和CO的选择性,工业生成CH3OOCCOOCH3时,选择140℃效果最好
D.130℃时,CO的选择性最高,说明CO生成CH3OOCCOOCH3的转化率最高
(4)120℃、常压时,CH3OOCCOOCH3+4H2![]() HOCH2CH2OH+2CH3OH反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。________
HOCH2CH2OH+2CH3OH反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。________
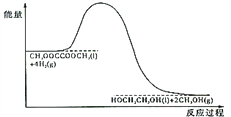
(5)研究证实,乙二醇、氧气可以在碱性溶液中形成燃料电池,负极的电极反应式是________________。
【答案】 4CO(g)+8H2(g)+O2(g)![]() 2HOCH2CH2OH(l)+2H2O(g)△H =(a+2b+2c)kJ·mol-1 < 100 增大 C
2HOCH2CH2OH(l)+2H2O(g)△H =(a+2b+2c)kJ·mol-1 < 100 增大 C 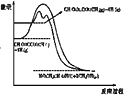 HOCH2CH2OH-10e-+14OH-==2CO32-+10H2O
HOCH2CH2OH-10e-+14OH-==2CO32-+10H2O
【解析】(1)反应I:4NO(g)+4CH3OH(g)+O2(g)![]() 4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
反应II:2CO(g)+2CH3ONO(g)![]() CH3OOCCOOCH3(l)+2NO(g) △H2=b kJ·mol-1
CH3OOCCOOCH3(l)+2NO(g) △H2=b kJ·mol-1
反应III:CH3OOCCOOCH3(1)+4H2(g)![]() HOCH2CH2OH(1)+2CH3OH(g) △H3 =c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g) △H3 =c kJ·mol-1
根据盖斯定律,将I+ II×2+III×2得4CO(g)+8H2(g)+O2(g)![]() 2HOCH2CH2OH(l)+2H2O(g)△H =(a+2b+2c)kJ·mol-1 ;该反应的△S<0,在较低的温度条件下自发进行的可能原因就是放热反应,即△H<0;故答案为:4CO(g)+8H2(g)+O2(g)
2HOCH2CH2OH(l)+2H2O(g)△H =(a+2b+2c)kJ·mol-1 ;该反应的△S<0,在较低的温度条件下自发进行的可能原因就是放热反应,即△H<0;故答案为:4CO(g)+8H2(g)+O2(g)![]() 2HOCH2CH2OH(l)+2H2O(g)△H =(a+2b+2c)kJ·mol-1 ;△H<0;
2HOCH2CH2OH(l)+2H2O(g)△H =(a+2b+2c)kJ·mol-1 ;△H<0;
(2)CO、CH3ONO各0.4mol在恒温、容积恒定为2L的密闭容器中发生反应II,达到平衡时CO的体积分数与NO的体积分数相等;令达到平衡时反应了的CO的物质的量为xmol,则反应了的CH3ONO的物质的量为xmol,生成的NO的物质的量为xmol,根据平衡时CO的体积分数与NO的体积分数相等可得:0.4-x=x,所以x=0.2mol,因此平衡常数k=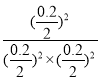 =100;若此时向容器中再通入0.4molNO,相当于增大NO浓度,平衡逆向移动,但是达到新平衡时NO的体积分数增大;故答案为:100 ;增大
=100;若此时向容器中再通入0.4molNO,相当于增大NO浓度,平衡逆向移动,但是达到新平衡时NO的体积分数增大;故答案为:100 ;增大
(3)A.根据表格数据,温度升高,空时收率先增大后减少,空时收率与CH3OOCCOOCH3的质量、反应时间、催化剂的体积三个因素有关,温度越高,建立平衡需要的反应时间越少,不能判断CH3OOCCOOCH3的质量的变化,也就无法判断反应的焓变,A错误;B.根据数据,温度升高,CO的选择性先逐渐降低,后又升高,说明反应温度在150℃时副反应较多,随着温度升高,催化剂活性可能逐渐增强,对CO的选择性又逐渐升高,B错误;C.在140℃时空时收率达到最高,CO的选择性也较高,副反应较少,因此工业生成CH3OOCCOOCH3时,选择140℃效果最好,C正确;D.130℃时,CO的选择性最高,只能说明此时的副反应较少,不能说明CO生成CH3OOCCOOCH3的转化率是否最高,D错误;故选C。
(4)升高温度,反应速率加快,建立平衡的时间减少,加入催化剂,能够降低反应的活化能,反应速率加快,建立平衡的时间减少,但焓变不变;由于草酸二甲酯的沸点为164.5℃,因此升高温度至180℃,草酸二甲酯会发生气化,反应物的起始能量增大,但最终产物的能量不变,因此焓变增大,图像为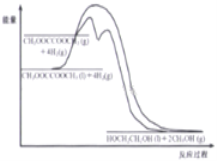 ,故答案为:
,故答案为: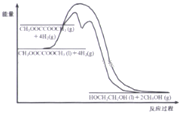 ;
;
(5)乙二醇、氧气在碱性溶液中形成燃料电池,乙二醇在负极发生氧化反应,负极的电极反应式为HOCH2CH2OH-10e-+14OH-==2CO32-+10H2O,故答案为:HOCH2CH2OH-10e-+14OH-==2CO32-+10H2O。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】2005年10月12日北京时间上午9时,中国酒泉卫星发射中心成功将“神舟6号”飞船送入太空,这一壮举又一次受到世界关注.火箭推进器中有强还原剂液体肼(N2H4)和强氧化剂液态双氧水.当它们混合时,即产生大量氮气和水蒸气并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应生成氮气和水蒸气,放出256.652kJ的热量.
(1)反应的热化学方程
(2)又已知H2O(l)=H2O(g)△H=44kJ.mol﹣1 . 则16g液态肼与足量的液态双氧水反应生成氮气和液态水时放出的热量是kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大优点是 .
(4)燃料电池在航天器得到大量应用;科研人员新近开发出一种由甲醇、氧气以及强碱作电解质溶液的新型手机电池,充电一次可供手机连续使用一个月,据此请回答以下问题:
①甲醇是极,电极反应
②电池反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药狼巴草的成分之一M具有清炎杀菌作用,M的结构简式如图所示: 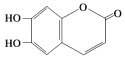 ,下列叙述正确的是( )
,下列叙述正确的是( )
A.M的分子式为C9H6O4
B.1 mol M最多能与2 mol Br2发生反应
C.1 molM最多能与4 mol氢氧化钠反应
D.M既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学在实验室用图甲装置制取乙酸乙酯。回答下列问题:

(1)实验中采用小火加热的目的是__________。
(2)加热A—会儿后,发现忘记加碎瓷片,应采取的正确操作是__________。
(3)浓硫酸的作用是__________。
(4)乙同学采用图乙装罝,图中球形干燥管除起冷凝作用外,另一要重用是__________。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是__________。
(6)下列描述能说明乙醇与乙酸的酯化反应己达到化学平衡状态的有(填序号)____。
①单位时间里生成1mol CH3COOCH2CH3的同时生成1 mol H2O
②单位时间里生成1mol CH3COOCH2CH3的同时消耗1mol CH3COOH
③单位时间里消耗1molCH3CH2OH的同时消耗1 mol CH3COOH
④混合物中各物质的浓度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃A能使溴的四氣化碳溶液褪色,其密度为相同条件下H2密度的14倍,完全燃烧产生等物质的里的CO2和H2O, A有如下转化关系,回答下列问题:
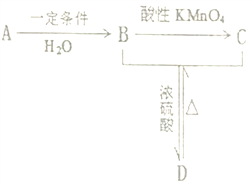
(1)A 的结构简式_______;B中含有的官能团名称______。
(2)A→B的反应类型为_______; C中含有的化学键类型_______。
(3)写出B+C→D的化学方程式_______;
(4)比A多一个碳的A的同系物与HCl气体反应得到的产物的同分异构体有_________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修5——有机化学基础】以芳香族化合物A和有机物D为原料,制备异戊酸薄荷醇酯(M)和高聚物(N)的一种合成路线如下图所示(部分反应条件已省略):

已知: I.A→B的原了利用率为100%;
II. ![]() (R1、R2表示氢原子或烃基)。
(R1、R2表示氢原子或烃基)。
请回答下列问题:
(1)用系统命名法对G命名,其化学名称为______________________。
(2)E的结构简式为____________________________。
(3)A→B的反应类型为_______。B分子中最多有____个原子共平面。
(4)C+G→M的化学方程式为_____________________________________。
(5)同时满足下列条件的B的同分异构体有______种(不考虑立体异构)。
①苯环上连有两个取代基 ②能发生银镜反应
(6)参照上述合成路线和信息,以苯乙烯为原料(无机试剂任选),设计制备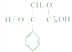 的合成路线______。
的合成路线______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氨的下列叙述中,不正确的是( )
A.液氨是纯净物
B.实验室制氨气的方法是加热NH4Cl
C.氨易液化,因此可用来作制冷剂
D.氨极易溶于水,因此可用来作喷泉实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G七种短周期主族元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍。A的一种原子中,质量数与质子数之差为零。D元素原子的最外层电子数为m,次外层电子数为n。E元素原子的L层上电子数为(m+n),M层上电子数为![]() 。F与D同主族。请回答下列问题:
。F与D同主族。请回答下列问题:
(1)B元素在周期表中的位置是________。
(2)C与E形成的化合物E3C属于________(填“原子”“离子”或“分子”)晶体。
(3)简单D离子和E离子的半径由大到小____________(填离子符号)
(4)B和D简单气态氢化物的稳定性; _______<_______(填化学式)
(5)F的一种氧化物中氧的质量分数为50%,写出该氧化物与G单质水溶液反应的化学方程式:__________________________________________________。
(6)已知:甲+H2O→丙+丁,该反应不是氧化还原反应。若甲是由N和Cl元素组成的化合物,其分子结构模型如下图所示,丙具有漂白性。则甲中氯元素的化合价是________,丁与H2O有相同的电子总数,则丁的结构式为________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅及其化合物在材料领域中应用广泛。下列叙述正确的是( )
A.晶体硅可做光导纤维
B.SiO2 可与水反应制备硅胶
C.玻璃、水泥、陶瓷都是硅酸盐产品
D.SiO2 与 NaOH 和 HF 均可反应,属于两性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com