
【题目】(1)写出表示含有8个质子,10个中子的原子的化学符号:__________。
(2)根据下列微粒回答问题:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、37Cl2
、37Cl2
①以上8种微粒共有________种核素,共________种元素。
②互为同位素的是________________。
③中子数相等的是_______________。
(3)相同物质的量的14CO与18O2的质量之比为_________。
【答案】![]() 6 5 11H、
6 5 11H、![]() 、
、![]() 14C、16O 5:6
14C、16O 5:6
【解析】
(1)表示含有8个质子,10个中子的原子的化学符号为![]() 。
。
(2)①核素是指具有一定数目质子和一定数目中子的一种原子,核素种类由质子数和中子数共同决定的。是具有相同质子数(核电荷数)的同一类原子的总称,决定元素的种类是质子数。
②具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素。
③中子数=质量数-质子数。
(3)14CO与18O2相对分子质量分别为:30和36,故相同物质的量的14CO与18O2的质量之比为5:6。
(1)表示含有8个质子,10个中子的原子的化学符号为![]() ,故答案为:
,故答案为:![]() 。
。
(2)①核素是指具有一定数目质子和一定数目中子的一种原子,核素种类由质子数和中子数共同决定的,故以上8种微粒共有6种核素;是具有相同质子数(核电荷数)的同一类原子的总称,决定元素的种类是质子数,故共有5种元素,故答案为:6;5。
②具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素,互为同位素的是11H、![]() 、
、![]() ,故答案为:11H、
,故答案为:11H、![]() 、
、![]() 。
。
③中子数=质量数-质子数,14C、16O的中子数为8,故答案为:14C、16O。
(3)14CO与18O2相对分子质量分别为:30和36,故相同物质的量的14CO与18O2的质量之比为5:6,故答案为:5:6。


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是
A. 它是副族元素 B. 它是第六周期元素
C. 它的原子核内有63个质子 D. 它的一种同位素的核内有89个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)石墨晶体中C-C键的键角为_______。其中平均每个六边形所含的C原子数为______个。
(2)金刚石晶体中共价键形成C原子环,每个C被_______个环共用,每条C-C被______个环共用。
(3)CsCl晶体中每个Cs+周围有_______个Cl-,每个Cs+周围与它最近且距离相等的Cs+共有________个。
(4)白磷分子中的键角为__________,分子的空间结构为__________,每个P原子与___个P原子结合成共价键。
(5) 晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答。这个基本结构单元由_____个硼原子组成,共含有_____个B-B键。
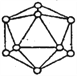
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。
已知:AlN + NaOH + H2O=NaAlO2+ NH3↑
(方案1)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
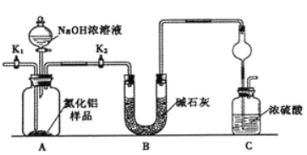
(1)上图C装置中球形干燥管的作用是________________________。
(2)完成以下实验步骤:组装好实验装置,首先检查装置的气密性,再加入实验药品。接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是__。
(3)若去掉装置B,则导致测定结果________(填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见__________________________。
(方案2)按以下步骤测定样品中A1N的纯度:
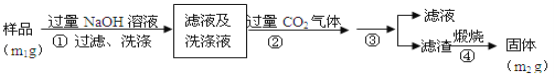
(4)步骤②生成沉淀的离子方程式为_________________________________。
(5)A1N的纯度是___________(用m1、m2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质(试样中括号内的物质是杂质)时,选用的试剂正确的是( )
A | B | C | D | |
试样 | Na2CO3(NaHCO3) | FeCl2(FeCl3) | Fe(Al) | CO2(SO2) |
除杂试剂 | 澄清石灰水 | NaOH溶液 | NaOH溶液 | 饱和NaHSO3溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaBH4燃料电池具有理论电压高、能量密度大等优点。已知,能量密度=电池输出电能/燃料质量(已知电子的电荷量为1.6×10-19C),以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是

A. 每消耗2.24 L O2(标准状况)时,A电极的质量减轻12.8 g
B. 离子交换膜应为阳离子交换膜,Na+由左极室向右极室迁移
C. 该燃料电池的负极反应式为BH4-+8OH--8e-=BO2- + 6H2O
D. 若NaBH4 燃料电池的电压为U伏,则此电池的能量密度为2.03×104UkJ·kg-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是

A. 位于第四周期
B. 质量数为34
C. 原子最外层有6个电子
D. 相对原子质量为78.96
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com