
分析 将燃烧产物全部依次通过无水氯化钙和碱石灰后,固体质量的增加依次为27g和44g,分别为水、二氧化碳的质量,则n(H2O)=$\frac{27g}{18g/mol}$=1.5mol,n(CO2)=$\frac{44g}{44g/mol}$=1mol,则n(C)=1mol×12g/mol=12g,m(H)=2×1.5mol×1g/mol=3g,m(O)=$\frac{23g-12g-3g}{16g/mol}$=8g,n(O)=0.5mol,则有机物中N(C):N(H):N(O)=1:3:0.5=2:6:1,最简式为C2H6O,应为乙醇,A在催化剂条件下能被氧气氧化成B,B的相对分子质量比A小2,则B为乙醛,A在酸性KMnO4溶液中能氧化成C,C为乙酸,结合对应有机物的性质解答该题.
解答 解:将燃烧产物全部依次通过无水氯化钙和碱石灰后,固体质量的增加依次为27g和44g,分别为水、二氧化碳的质量,则n(H2O)=$\frac{27g}{18g/mol}$=1.5mol,n(CO2)=$\frac{44g}{44g/mol}$=1mol,则n(C)=1mol×12g/mol=12g,m(H)=2×1.5mol×1g/mol=3g,m(O)=$\frac{23g-12g-3g}{16g/mol}$=8g,n(O)=0.5mol,则有机物中N(C):N(H):N(O)=1:3:0.5=2:6:1,最简式为C2H6O,应为乙醇,A在催化剂条件下能被氧气氧化成B,B的相对分子质量比A小2,则B为乙醛,A在酸性KMnO4溶液中能氧化成C,C为乙酸,
(1)由以上分析可知A的分子式为C2H6O,结构简式为CH3CH2OH,故答案为:C2H6O;CH3CH2OH;
(2)乙醇在催化剂(Cu或Ag)的作用下发生催化氧化生成乙醛,反应方程式为2CH3CH2OH+O2$→_{△}^{Cu}$CH3CHO+2H2O.
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$CH3CHO+2H2O;
(3)乙醇和乙酸在浓硫酸作用下加热发生酯化反应生成乙酸乙酯,也为取代反应,反应的方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;酯化(或取代)反应.
点评 本题考查有机物的推断,为高频考点,侧重于有机物燃烧的规律的计算,注意把握有机物的结构特点以及官能团的转化,结合对应有机物的性质解答该题,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 是烃 | B. | 不能在空气中燃烧 | ||
| C. | 常温下呈固态 | D. | 可能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
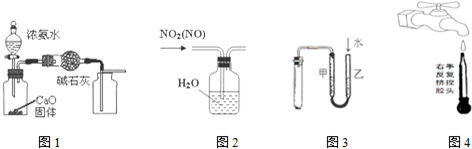
| A. | 用图1装置制取并收集干燥纯净的NH3 | |
| B. | 用图2所示装置可除去NO2中的NO | |
| C. | 用图3所示装置检验装置的气密性 | |
| D. | 图④是实验室洗涤胶头滴管的操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
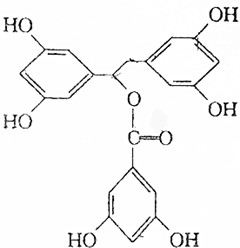 某有机物K的结构简式如图:等物质的量的K分别与足量的氢氧化钠溶液、足量氢气(镍、加热)、足量的溴水反应,消耗NaOH、H2、Br2的物质的量之比为( )
某有机物K的结构简式如图:等物质的量的K分别与足量的氢氧化钠溶液、足量氢气(镍、加热)、足量的溴水反应,消耗NaOH、H2、Br2的物质的量之比为( )| A. | 7:9:9 | B. | 8:9:9 | C. | 7:10:9 | D. | 7:9:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.| 编号 | 反应物 | 催化剂 |
| ① | 10mL 2%H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 10mL 5%H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5% 5H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5%H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| B. | 常温下,pH=2的CH3COOH溶液和H2SO4溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离出的c(H+)不相等 | |
| C. | 常温下将浓度为0.1 mol•L-1的HF溶液加水不断稀释,溶液中$\frac{c({H}^{+})}{c(HF)}$的值始终保持增大 | |
| D. | 常温下0.1 mol•L-1的下列溶液①NH4Fe(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中,c(NH4+)由大到小的顺序是:②>①>④>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HC1的电子式: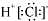 | B. | 乙烯分子的结构简式:CH2CH2 | ||
| C. | S2-的原子结构示意图: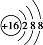 | D. | H2O2的电子式: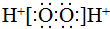 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com