
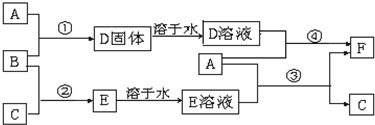
���� A����;���Ľ�������AΪFe��D��Һ�еμ�KSCN��Һ�Ժ�ɫ����D�к��������ӣ�B�dz������嵥�ʺ�Fe��Ӧ�������������Σ�֤��B����ǿ�����ԣ�����BӦΪCl2��E��ҺΪ����ǿ��ΪHCl�������Ƴ�DΪFeCl3��FΪFeCl2�����ת����ϵͼ��֪��Fe��E��Һ��Ӧ����FeCl2��C����EΪHCl��CΪH2������ϻ�ѧ���P��Ӧ�����������
��1��BΪ������FΪ�Ȼ�������Һ��
��2���ڢ۲���ӦΪFe�����ᷴӦ�����Ȼ�������������
��3���ڢܲ���ӦΪFe���Ȼ�����Ӧ�����Ȼ�������
��4��FΪFeCl2������Һ�е���NaOH��Һ��Ӧ����������������ɫ���������ձ���������ɫ����������������
��� �⣺A����;���Ľ�������AΪFe��D��Һ�еμ�KSCN��Һ�Ժ�ɫ����D�к��������ӣ�B�dz������嵥�ʺ�Fe��Ӧ�������������Σ�֤��B����ǿ�����ԣ�����BӦΪCl2��E��ҺΪ����ǿ��ΪHCl�������Ƴ�DΪFeCl3��FΪFeCl2�����ת����ϵͼ��֪��Fe��E��Һ��Ӧ����FeCl2��C����EΪHCl��CΪH2��
��1���������ƶϿ�֪��BΪCl2��FΪ�Ȼ�������
�ʴ�Ϊ��Cl2���Ȼ�������
��2���ڢ۲���ӦΪFe�����ᷴӦ�����Ȼ���������������ѧ����ʽΪFe+2HCl=FeCl2+H2����
�ʴ�Ϊ��Fe+2HCl=FeCl2+H2����
��3���ڢܲ���ӦΪFe���Ȼ�����Ӧ�����Ȼ����������ӷ�ӦΪ2Fe3++Fe=3Fe2+���۲쵽����Ϊ��Һ�ɻ�ɫ��Ϊdz��ɫ��
�ʴ�Ϊ����Һ�ɻ�ɫ��Ϊdz��ɫ��2Fe3++Fe=3Fe2+��
��4��FΪFeCl2������Һ�е���NaOH��Һ��Ӧ����������������ɫ���������ձ���������ɫ�����������������۲쵽����Ϊ�����ɻҰ�ɫ������������ɻ���ɫ������ɺ��ɫ��
�ʴ�Ϊ�������ɻҰ�ɫ������������ɻ���ɫ������ɺ��ɫ��
���� ���⿼��������ƶϣ��������ʵ����ʼ�ת����ϵͼ���ƶ������ǽ��Ĺؼ���ע��A��DΪ������ͻ�ƿڣ���Ŀ�ѶȲ���


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ�����Ƶĵ��� | B�� | һ�����ƵĻ����� | ||
| C�� | һ��������Ԫ�أ����ܺ��м�Ԫ�� | D�� | һ�����м�Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
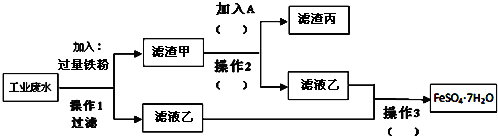
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Cu2O�ڷ�Ӧ�б����� | |
| B�� | Cu2S�ڷ�Ӧ�м������������ǻ�ԭ�� | |
| C�� | SO2���������� | |
| D�� | ����Ӧ��ת��12mol���ӣ�������6mol Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=8.0��KHS��Һ�У�c��K+����c��HS-����c��OH-����c��S2-����c��H+�� | |
| B�� | 1.0 mol•L-1Na2C2O4��Һ��c��OH-��=c��HC2O4-��+c��H+��+c��H2C2O4�� | |
| C�� | ����������Һ�еμ�ϡ����õ���pH=5�Ļ����Һ��c��Na+��=c��NO3-�� | |
| D�� | ��0.2 mol•L-1��ijһԪ��HA��Һ��0.1 mol•L-1NaOH��Һ�������Ϻ���ҺpH����7����Ӧ��Ļ��Һ�У�c��OH-��+c��A-��=c��H+��+c��HA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ѥ���ͷ��̻��������˺��ء��ơ��ơ�ͭ�Ƚ���Ԫ�صĵ��ʻ��� | |
| B�� | ʳ��ֲ���͵���Ҫ�ɷ��Ǹ�֬���������������������Ӫ������ | |
| C�� | ���������������Һ������������Һ���Ҵ���Һ������������ɱ������ԭ����ͬ | |
| D�� | PM2.5��ָ������ֱ��С�ڻ����2.5�Ŀ������ΰ��ȼ����ķ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe��OH��3��������ֱ����1nm��100 nm֮�� | |
| B�� | ����������������ɢϵ�ı����������ж����ЧӦ | |
| C�� | Fe��OH��3�����л�������FeCl3�����Բ�ȡ���˵ķ������� | |
| D�� | ������FeCl3��Һ�μӵ���ˮ�г�ʱ������Ƶ�Fe��OH��3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com