
【题目】关于下列各装置图的叙述中,错误的是:
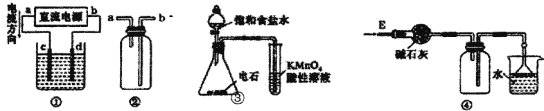
A. 装置①用来电解饱和食盐水,c电极产生的气体能使湿润的淀粉KI试纸变蓝
B. 装置②可用于收集H2、NH3、Cl2、HCl、NO2
C. 装置③检查乙炔的还原性(实验室是由饱和食盐水与电石制乙炔,产生的混合气体除乙炔外,常含有H3P ,H2S等杂质气体)
D. 装置④可用于干燥、收集氨气、并吸收多余的氨气
【答案】C
【解析】
A. 外电路电流从原电池的正极流出,所以a是正极,b是负极;电解饱和食盐水时, c电极为电解池的阳极,溶液中氯离子在此极发生氧化反应生成能使湿润的淀粉KI试纸变蓝的气体氯气,故A正确;
B. H2、NH3、Cl2、HCl、NO2可以采用排空气法来收集,收集时, H2、NH3导管是短进长出, Cl2、HCl、NO2的收集是导管长进短出,故B正确;
C.乙炔中含有杂质硫化氢等,硫化氢具有还原性,能使酸性高锰酸钾溶液褪色,影响到乙炔的还原性的检验,故C错误;
D.,氨气的收集采用向上排空气法,导管可以短进长出,用碱石灰来干燥,用水来吸收时,要防止倒吸,故D正确;
正确选项:C。


科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔(C2H2)是制造草酸、乙醛、醋酸等有机化合物的基本原料。
(1)某小组同学以电石(主要成分为CaC2,含少量CaS及Ca3P2等杂质)为原料,利用下图所示实验装置(夹持装置略去,下同)制备C2H2。

①仪器a的名称为__________________________。
②CaC2的电子式为________________________________。
③装置B中的NaClO溶液能将H2S、PH3氧化为硫酸、磷酸,本身被还原为NaCl。其中PH3被氧化的离子方程式为________________________________。
(2)该小组同学通过查阅文献资料得知:用Hg(NO3)2作催化剂时,浓硝酸能将乙炔气体氧化为草酸(H2C2O4),实验装置如下图所示。

①装置E的作用是_________________________________________。
②装置D中生成H2C2O4的化学方程式为_________________________________。
③装置D中锥形瓶内的液体经过___________(填操作名称)、洗涤、干燥等步骤得到H2C2O4·2H2O晶体。
(3)该小组同学测定了晶体中H2C2O4·2H2O的质量分数,实验步骤如下:
i.准确称取mg晶体,加入适量的蒸馏水溶解,再加入少量稀硫酸;
ii.将i所得溶液用c mol/LKMnO4标准溶液进行滴定,滴定时KMnO4被还原为Mn2+,滴定至终点时消耗标准溶液VmL。
①滴定过程中发现褪色速率先慢后明显加快,除反应放热外,还可能的原因是____________。
②晶体中H2C2O4·2H2O的质量分数为_________(用含m、c、V的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图是从元素周期表中截取下来的,甲、乙、丙为短周期主族元素,下列说法中正确的是( )
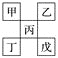
A. 丁一定是金属元素,其金属性比丙强
B. 丙的最高价氧化物水化物显强酸性
C. 乙的氢化物是以分子形式存在,且分子间存在氢键
D. 戊的原子序数一定是甲的5倍,且原子半径比甲大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时,水的电离达到平衡:H2O![]() H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是
A.将纯水加热到950C时,Kw变大,pH不变,水仍呈中性
B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小
C.向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,KW不变
D.向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:
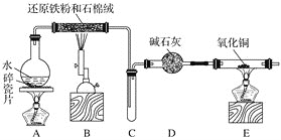
(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_________________________。
(2)装置B中发生反应的化学方程式是____________________________________,该反应中氧化剂是__________,氧化产物是__________________。
(3)D的作用是__________________________________。
(4)E中的实验现象是____________________________。
(5)A、B两个装置中应先点燃________________处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿斯匹林的制备装置和反应原理如下:
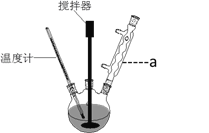
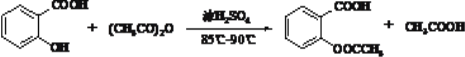
已知乙酸酐(CH3C0)2O在水中会发生水解反应生成乙酸。
实验步骤:
①开启水浴恒温槽的电源,使水浴温度控制在85℃-90℃。
②在三口瓶中加入5g水杨酸,14ml(15g)乙酸酐(CH3C0)2O,1.8ml浓硫酸。
③在水浴中,搅拌反应15min,冷却至室温,在瓶中加入70ml水,继续搅拌5min,再放在冷水浴中静置5—10min,加入冰块,在冰水浴中静置10—20min,冷却结晶,抽滤,用少量冰水洗涤2次。
④将晶体放在250ml烧杯中,并加入70ml饱和碳酸氢钠溶液,搅拌到无二氧化碳放出为止。抽滤除去聚合物固体。
⑤将滤液放在250ml烧杯中,边搅拌边慢慢滴入18%盐酸,直至PH值为1.5。烧杯放入冰水浴中冷却,直至结晶完全。真空抽滤,用少量冰水洗涤二次,得粗产品。
⑥粗产品放入150ml烧杯中,加入20ml无水乙醇,搅拌,缓慢加热,直至晶体溶解,再加入40ml水,在室温中静置,再放入冰水浴中冷却,直至结晶完全。真空抽滤,用少量无水乙醇-水(1:2,v/v)溶液洗涤,烘干,得产品。称量,计算产率。
回答以下问题:
(1)仪器a的名称为_________________
(2)反应容器干燥无水的原因是__________________________________。加入浓硫酸的目的是______________________________________。水浴加热的目的是__________________________
(3)本实验含有两个六元环和一个八元环的副产物的结构简式为__________________。
(4)加入70ml饱和碳酸氢钠溶液的目的是__________________________________。把碳酸氢钠换为氢氧化钠将使产品因________________________而损失。
(5)将滤液边搅拌边慢慢滴入18%盐酸利用了______________________________的原理。
(6)水杨酸可以在各步纯化过程和产物的重结晶过程中被除去,检验水杨酸除尽的方法是____________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com