
ĻĀĮŠ³żŌÓÖŹµÄ²Ł×÷ÖŠ²»ÕżČ·µÄŹĒ
A£®Ģś·ŪÖŠ»ģÓŠĀĮ·Ū£ŗ¼ÓČė¹żĮæÉÕ¼īČÜŅŗ³ä·Ö·“Ó¦ŗó¹żĀĖ
B£®FeCl2ČÜŅŗÖŠ»ģÓŠFeCl3£ŗ¼ÓČė¹żĮæĢś·Ū³ä·Ö·“Ó¦ŗó¹żĀĖ
C£®Na2CO3¹ĢĢåÖŠ»ģÓŠÉŁĮæNaHCO3£ŗ¼ÓČėŹŹĮæNaOHČÜŅŗ
D£®ĀČĘųÖŠ»ģÓŠÉŁĮæĀČ»ÆĒāĘųĢå£ŗ½«»ģŗĻĘųĢåĶعżŹ¢±„ŗĶŹ³ŃĪĖ®µÄĻ“ĘųĘæ
 »ĘøŌ¾µäȤĪ¶æĪĢĆĻµĮŠ“š°ø
»ĘøŌ¾µäȤĪ¶æĪĢĆĻµĮŠ“š°ø Ęō¶«Š”Ģā×÷Ņµ±¾ĻµĮŠ“š°ø
Ęō¶«Š”Ģā×÷Ņµ±¾ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”ŗ¼ÖŻŹŠøßŅ»ÉĻŃ§ĘŚĘŚÄ©Ä£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ļņŗ¬ÓŠFe2+”¢I-”¢Br-µÄČÜŅŗÖŠĶØČėŹŹĮæĀČĘų£¬ČÜŅŗÖŠø÷ÖÖĄė×ÓµÄĪļÖŹµÄĮæ±ä»ÆČēĻĀĶ¼ĖłŹ¾”£ÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø £©
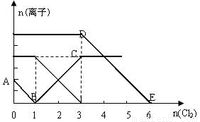
A£®»¹ŌŠŌI->Fe2->Br-
B£®Ō»ģŗĻČÜŅŗÖŠc(FeBr2) = 4mol/L
C£®µ±ĶØČėCl2 2molŹ±£¬ČÜŅŗÖŠŅŃ·¢ÉśµÄĄė×Ó·“Ó¦æɱķŹ¾ĪŖ£ŗ2Fe2+ + 2I- + 2Cl2 ”ś 2Fe3+ + I2 + 4 Cl-
D£®ŌČÜŅŗÖŠn(Fe2+) £ŗn(I-) £ŗn(Br-) = 2 £ŗ1 £ŗ3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”Äž²ØŹŠøßŅ»ÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ö»ÓĆŅ»ÖÖŹŌ¼ĮĒų±šNa2SO4”¢MgCl2”¢FeCl2”¢Al2£ØSO4£©3”¢£ØNH4£©2SO4ĪåÖÖČÜŅŗ, ÕāÖÖŹŌ¼ĮŹĒ
A£®Ba£ØOH£©2 B£®H2SO4 C£®NaOH D£®AgNO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”Äž²ØŹŠ°ĖŠ£øßŅ»ÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĻņŹ¢ÓŠKIČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėÉŁŠķCCl4ŗóµĪ¼ÓĀČĖ®£¬CCl4²ć±ä³É×ĻÉ«”£Čē¹ū¼ĢŠųĻņŹŌ¹ÜÖŠµĪ¼ÓĀČĖ®£¬Õńµ“£¬CCl4²ć»įÖš½„±äĒ³£¬×īŗó±ä³ÉĪŽÉ«”£
Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£Ø1£©Š“³ö²¢ÅäĘ½CCl4²ćÓÉ×ĻÉ«±ä³ÉĪŽÉ«µÄ»Æѧ·“Ó¦·½³ĢŹ½(Čē¹ūĻµŹżŹĒ1£¬²»ÓĆĢīŠ“)£ŗ

£Ø2£©Õūøö¹ż³ĢÖŠµÄ»¹Ō¼ĮŹĒ________________”£
£Ø3£©°ŃKI»»³ÉKBr£¬ŌņCCl4²ć±ä³É________É«£¬¼ĢŠųµĪ¼ÓĀČĖ®£¬CCl4²ćµÄŃÕɫƻӊ±ä»Æ”£Cl2”¢HIO3”¢HBrO3Ńõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ ”£
£Ø4£©¼ÓµāŃĪÖŠŗ¬µāĮæĪŖ25.4mg”«50 mg/kg”£ÖĘČ”¼ÓµāŃĪ(ŗ¬KIO3µÄŹ³ŃĪ)1000 kg£¬ČōÓĆKIÓėCl2·“Ó¦ÖĘKIO3£¬ÖĮÉŁŠčŅŖĻūŗÄCl2 L(±ź×¼×“æö)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”Äž²ØŹŠ°ĖŠ£øßŅ»ÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĶ¼ĖłŹ¾ŹĒŃéÖ¤ĀČĘųŠŌÖŹµÄĪ¢ŠĶŹµŃ飬a”¢b”¢d”¢eŹĒ½žÓŠĻą¹ŲČÜŅŗµÄĀĖÖ½”£ĻņKMnO4¾§ĢåµĪ¼ÓŅ»µĪÅØŃĪĖįŗó£¬Į¢¼“ÓĆĮķŅ»ÅąŃųĆóæŪŌŚÉĻĆę”£
¼ŗÖŖ£ŗ2KMnO4+16HCl=2KCl+5Cl2”ü+2MnCl2+8H2O

¶ŌŹµŃéĻÖĻóµÄ”°½āŹĶ»ņ½įĀŪ”±ÕżČ·µÄŹĒ
Ń”ĻīŹµŃéĻÖĻó½āŹĶ»ņ½įĀŪ
Aa“¦±äĄ¶£¬b“¦±äŗģ×ŲÉ«Ńõ»ÆŠŌ£ŗCl2>Br2>I2
Bc“¦Ļȱäŗģ£¬ŗóĶŹÉ«ĀČĘųÓėĖ®Éś³ÉĮĖĖįŠŌĪļÖŹ
Cd“¦Į¢¼“ĶŹÉ«ĀČĘųÓėĖ®Éś³ÉĮĖĘư׊ŌĪļÖŹ
De“¦±äŗģÉ«»¹ŌŠŌ£ŗFe2£« > Cl£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”Äž²ØŹŠ°ĖŠ£øßŅ»ÉĻѧʌʌĩĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷ÖŠ“ķĪóµÄŹĒ
A£®¹żĀĖ²Ł×÷Ź±Čē¹ūÓŠ±ŲŅŖæÉŅŌÓĆÕōĮóĖ®Ļ“µÓĀĖÖ½ÉĻµÄ³Įµķ2-3“Ī
B£®ÕōĮó²Ł×÷Ź±£¬Ó¦Ź¹ĪĀ¶Č¼ĘĖ®ŅųĒņ²åČėŅŗĢ¬»ģŗĻĪļÖŠ
C£®·ÖŅŗ²Ł×÷Ź±£¬·ÖŅŗĀ©¶·ÖŠĻĀ²ćŅŗĢå“ÓĻĀæŚ·Å³ö£¬ÉĻ²ćŅŗĢå“ÓÉĻæŚµ¹³ö
D£®ŻĶČ”²Ł×÷Ź±£¬ŅŖ²»¶ĻÕńŅ”·ÖŅŗĀ©¶·²¢·ÅĘų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ĻĀѧʌµŚŅ»“ĪÖŹĮæ¼ģ²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ĘĖćĢā
ĻņĶʬ֊¼ÓČė115mLijÅØ¶ČµÄĮņĖį£¬ŌŚ¼ÓČČĢõ¼žĻĀ·“Ó¦£¬“żĶʬȫ²æČܽāŗ󣬽«ĘäČÜŅŗĻ”ŹĶµ½500mL£¬ŌŁ¼ÓČė×ćĮæŠæ·Ū£¬Ź¹Ö®³ä·Ö·“Ó¦£¬ŹÕ¼Æµ½2£®24L£Ø±ź×¼×“æö£©ĘųĢ唣¹żĀĖ²ŠĮō¹ĢĢ壬øÉŌļŗó³ĘĮæ£¬ÖŹĮæ¼õĒįĮĖ7£®5g”£
£Ø1£©Ēó²Ī¼Ó·“Ó¦µÄŠæ·ŪµÄĪļÖŹµÄĮæ
£Ø2£©ŌĮņĖįµÄĪļÖŹµÄĮæÅØ¶Č”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”øßŅ»ĻĀѧʌµŚŅ»“ĪÖŹĮæ¼ģ²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ČēĶ¼ŹĒÄ£ÄāĀČ¼ī¹¤ŅµÉś²śÖŠ¼ģ²éĀČĘųŹĒ·ńŠ¹Ā©µÄ×°ÖĆ£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ

A£®ÉÕĘæÖŠĮ¢¼“³öĻÖ°×ŃĢ
B£®ÉÕĘæÖŠĮ¢¼“³öĻÖŗģ×ŲÉ«
C£®ÉÕĘæÖŠ·¢ÉśµÄ·“Ó¦±ķĆ÷³£ĪĀĻĀ°±ĘųÓŠ»¹ŌŠŌ
D£®ÉÕ±ÖŠµÄČÜŅŗŹĒĪŖĮĖĪüŹÕÓŠŗ¦ĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗÓÄĻŹ”פĀķµźŹŠøßŅ»ÉĻѧʌĖÄŠ£ĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø5·Ö£© ŌŚĶ¬ĪĀĶ¬Ń¹ĻĀ£¬Ķ¬Ģå»żµÄ¼×Ķé£ØCH4£©ŗĶ¶žŃõ»ÆĢ¼·Ö×ÓŹżÖ®±ČĪŖ””””””£¬ĪļÖŹµÄĮæÖ®±ČĪŖ”” £¬Ō×Ó×ÜŹżÖ®±ČĪŖ”” ””£¬ÖŹĮæÖ®±ČĪŖ”” £¬ĆܶČÖ®±ČĪŖ”” ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com