
分析 同温同压下,同体积的气体,质量之比等于摩尔质量之比,据此计算A的摩尔质量,确定A的相对分子质量,根据n=$\frac{m}{M}$计算A的物质的量,利用N=nNA计算A的分子数目;同温同压下,相同体积的任何气体含有相同数目的分子数,根据n=$\frac{V}{Vm}$=$\frac{m}{M}$,结合分子的构成进行计算.
解答 解:同温同压下,同体积的气体,质量之比等于摩尔质量之比,故0.2g:3.4g=2g/mol:M(A),解得M(A)=34g/mol,3.4gA的物质的量为$\frac{3.4g}{34g/mol}$=0.1mol,A的分子数目为0.1mol×NAmol-1=0.1NA;
同温同压下,气体的Vm相等,由n=$\frac{V}{Vm}$=$\frac{m}{M}$可知,同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比与气体的摩尔质量成正比,则
m(NH3):m(H2S)=M(NH3):M(H2S)=17g/mol:34g/mol=1:2;
设气体的质量都为m,由n=$\frac{V}{Vm}$=$\frac{m}{M}$可知,同质量的氨气和硫化氢(H2S)气体在相同条件下的体积比与气体的物质的量呈正比,则
v(NH3):V((H2S)=$\frac{mg}{17g/mol}$:$\frac{mg}{34g/mol}$=2:1,所含原子个数比为2×4:1×3=8:3;
故答案为:16;0.1NA;1:2; 2:1; 8:3.
点评 本题考查阿伏伽德罗定律及推论、常用化学计量的有关计算,难度不大,注意物质的量的有关计算公式的运用.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气是非电解质,氨水是电解质 | |
| B. | 氢氧化铁胶体可以发生丁达尔现象 | |
| C. | 摩尔和物质的量均是联系宏观和微观数量的物理量 | |
| D. | 硫酸氢钠能解离出H+,与碳酸钠反应有二氧化碳生成,因此属于酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH=CH2与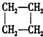 | B. |  与 与 | ||
| C. | 甲苯和二甲苯 | D. | CH2═CH-CH═CH2和CH-CH2-CH2-C≡CH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示,2min后反应达到平衡.由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示,2min后反应达到平衡.由图中数据分析:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com