
 置换反应的通式可用如图表示,单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
置换反应的通式可用如图表示,单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:分析 (1)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,A为水,甲为Na,生成B为NaOH;
(2)工业上利用置换反应原理制备一种半导体材料,为C与二氧化硅反应生成Si、CO;
(3)若气体单质乙能在空气中燃烧,化合物B为黑色磁性晶体,B为四氧化三铁,则甲为Fe,A为水蒸气,以此来解答.
解答 解:(1)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,A为水,甲为Na,生成B为NaOH,该反应的离子反应方程式为2Na+2H2O=2Na++2OH-+H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(2)工业上利用置换反应原理制备一种半导体材料,为C与二氧化硅反应生成Si、CO,该反应为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(3)若气体单质乙能在空气中燃烧,化合物B为黑色磁性晶体,B为四氧化三铁,则甲为Fe,A为水蒸气,该反应为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应与现象、相互转化为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,焰色反应、半导体材料、黑色固体为推断的突破口,题目难度不大.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 分离出CO(NH2)2 | C. | 缩小容器体积 | D. | 使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
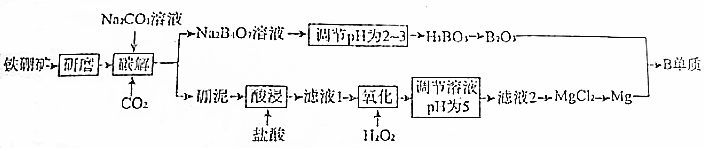
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
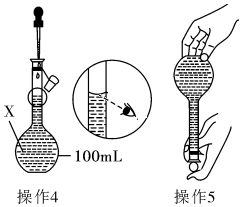 某同学欲配制100mL 0.10mol•L-1的CuSO4溶液.以下操作1~5是其配制的过程及示意图:
某同学欲配制100mL 0.10mol•L-1的CuSO4溶液.以下操作1~5是其配制的过程及示意图:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2 (g)+O2(g)=2H2O(l) | B. | H2(g)+Cl2 (g)=2HCl(g) | ||
| C. | (NH4)2CO3(s)=NH4HCO3 (s)+NH3(g) | D. | Cu(s)+Cl2 (g)=CuCl2 (s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
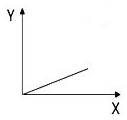
| A. | 一定状况下,气体摩尔体积(Y)与该气体的物质的量(X)的关系 | |
| B. | 在光照情况下,一定体积的饱和氯水的pH(Y)随时间(X)的关系 | |
| C. | 100℃,1个大气压下,按体积比1:1混合的CO2和H2O(g)混合气通过足量Na2O2粉末,固体增加的质量(Y)与混合气体积(X)的关系 | |
| D. | 向AlCl3溶液中滴加NaOH溶液至过量,生成Al(OH)3 的物质的量(Y)与消耗NaOH的物质的量(X)的关系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com