
下列有关说法体现了化学与生产、生活、社会的密切关系。其中不正确的是
A.绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物
B.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰
C.停车场安装催化光反应设施,可使汽车尾气中的CO和NOX反应生成无毒气体
D.氮化硅陶瓷、氧化铝陶瓷、光导纤维等属于新型无机非金属材料
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 18g D2O含有的电子数为10NA
B. 标准状况下,11.2 L SO3中含有的分子数为0.5 NA
C. 7.8 g Na2O2晶体中含有的阴离子数为0.1 NA
D. 常温常压下,44 g CO2气体含有氧原子的个数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol・L―1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第__________周期第__________族,它的最高价氧化物的化学式为____________。
(2)A元素是_________,B元素是________,D元素是_______。(填名称)
(3)A与D形成稳定化合物的电子式是_____________,判断该化合物在空气中是否变质的简单方法是_______________________________。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
a molNa2O2和b molNaHCO3固体混合后,在密闭容器中加热到250℃,使其充分反应,当排出气体为两种气体时,a:b不可能为( )
|
| A. | 3:4 | B. | 4:5 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验装置进行相应实验,能达到实验目的的是
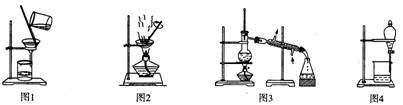
A.用图1所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒
B.用图2所示装置蒸发掉CuCl2溶液中部分水制得CuCl2·2H20晶体
C.用图3所示装置从CH3OH与C2H5OH的混合物中分离出乙醇
D.用图4所示装置从C2H5OH与C2H5OOCCH3的混合物中分离出乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A.HF稳定性比HCl强 B.Mg失电子能力比Ca弱
C.NaCl与NH4Cl含有的化学键类型相同 D.等物质的量的C2H6和H2O2含电子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是
A.由H+(aq)+OH-(aq)=H20(1) △H=-57.3 kJ·mol-1,可知含1 mo1 CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量为57.3 kJ
B.由C(石墨)=C(金刚石) △H=+1.9 kJ·mol-1,可知石墨比金刚石更稳定
C.由N2(g)+3H2(g)=2NH3(g) △H=-92.4 kJ·mol-1,可知将1 mol N2(g)和3 mol H2(g)置于密闭容器中充分反应后放出热量为92.4 kJ
D.由△G=△H-T△S可知,所有的放热反应都能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
在2A(g)+B(g) = 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.vA=0.5mol·L-1·s-1
B.vB=0.3 mol·L-1·s-1
C.vC=0.8 mol·L-1·s-11
D.vD=1.0 mol·L-1·s-11
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学用下图所示实验装置进行实验研究(图中a、b、c表示止水夹),请对其方案进行完善或评价。

(1)实验室将B、C、E相连后,以浓盐酸和 为原料可制取Cl2。
(2)利用实验室常用方法制取氯气,将A、C、E相连,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作如下,将现象①填入下表:
| 实验序号 | 实验操作 | 现象 |
| Ⅰ | 将氯水滴入品红溶液 | ① |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 |
②请你评价:
实验Ⅱ推出相应的结论是氯气与水反应的产物具有酸性,是否合理? ________________若不合理,请说明理由(若合理,无需填写):________________________________________。
(3)A、C、E相连,可设计一个简单的实验,以验证Cl-和Br-的还原性强弱,C中应放入的试剂是 。
(4)B、D、E装置相连后,在B中盛装浓硝酸和铜片,可制得NO2,欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹_______,再打开止水夹c,双手紧握(或微热)试管丁,使试管中气体逸出,NO2与水接触后观察到的现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com