
为测定气球内的气体成分,有的学生用超薄的气球按如图装置进行实验。开始时气球沉于烧杯底部,打开开关后,过一会儿气球从烧杯底部慢慢浮起,最后悬于烧杯口。气球内盛放的气体可能是( )xk|b|1
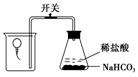
A.O2 B.H2
C.NH3 D.SO2
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
有关物质的转化关系如下图所示(部分物质和条件已略去)。B、C、E是常见气体;A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;G的焰色反应显黄色;I的溶液呈黄色。
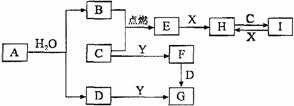 |
请回答下列问题:
⑴ F的化学式为________________。
⑵ E的电子式为________________。
⑶ 写出C与D溶液反应的化学方程式:___________________________________。
⑷ 写出Y和D溶液反应的离子方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献。已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应。(注:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2。)下列说法正确的是( )
A.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI 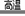 CeI4 + 2H2↑
CeI4 + 2H2↑
B.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + 2Fe2+ == Ce3+ + 2Fe3+
C.金属Ce保存时,应该隔绝空气和水
D.铈的四种核素136 58Ce、138 58Ce、140 58Ce、142 58Ce,它们互称为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下几种物质①熔融氯化钠 ②浓硫酸 ③Cu ④蔗糖 ⑤CH3COOH
⑥NaHCO3 ⑦酒精 ⑧液溴,填空回答:(填序号)
(1)以上物质中属于强电解质的是 ; 属于非电解质的是 ;
(2)写出⑤⑥在水中的电离方程式:⑤ ;⑥ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+
B.加入K3[Fe(CN)6]溶液,产生特征蓝色沉淀,则原溶液一定有Fe3+
C.加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO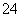
D.加入NaOH溶液,产生气体使湿润的红色石蕊试纸变蓝,则原溶液一定有NH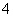
查看答案和解析>>
科目:高中化学 来源: 题型:
建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
NaNO2+HI―→NO+I2+NaI+H2O(未配平)
(1)上述反应的氧化剂是________;若有1 mol的还原剂被氧化,则反应中转移电子的数目是________。
(2)根据上述反应,可用试剂和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋。下列几组中最合适的是________(填序号)。
A.①② B.①②④
C.①②⑤ D.③⑤
(3)某工厂废液中含有2%~5%的NaNO2,直接排放会造成污染,采用NH4Cl能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为___________________________
________________________________________________________________________。
(4)采用烧碱处理硝酸工业尾气(NO、NO2)可以获得副产品NaNO2,变废为宝。若采用a L b mol/L的烧碱处理硝酸工业尾气,最多可以获得NaNO2的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
离子反应是中学化学中重要的反应类型.回答下列问题:
(1)人们常用图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为下左图.下右图为离子反应、氧化还原反应和置换反应三者之间的关系,则表示离子反应、氧化还原反应、置换反应的字母分别是________.

(2)将NaBr溶液加入AgCl沉淀中,产生AgBr黄色沉淀.从离子反应发生的条件分析,AgCl与AgBr相比较,溶解度较大的是________.
(3)离子方程式是重要的化学用语.下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点.
反应物从下列物质中选取:Na、Fe、H2O、H2SO4、HCl、NaOH、Ba(OH)2、CuCl2(已知2Na+2H2O===2NaOH+H2↑).
| 错误观点 | 离子方程式 | |
| ① | 所有的离子方程式均可以表示一类反应 | |
| ② | 所有酸碱中和反应均可表示为:H++OH-===H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组欲测定某品牌味精中氯化钠的含量。该小组的实验步骤如下:
①称取该味精样品10.0g放入烧杯中,并加适量蒸馏水完全溶解;
②加入过量的用硝酸酸化的硝酸银溶液(假定只有NaCl与AgNO3溶液反应)。
③过滤;
④用蒸馏水洗涤沉淀2~3次;
⑤将沉淀烘干、称量,测得其质量为5.74g;
请回答下列问题:
(1)上述实验步骤③操作中所用到的玻璃仪器有 。
(2)若此品牌味精包装袋上标注:“谷氨酸钠含量≥80.0% ,氯化钠含量≤20.0%”;(假设样品中不含其它杂质)。通过上述实验结果,可计算出样品中氯化钠的质量分数为 ,所以该样品 (填“合格”或“不合格”)。
(3)检验上述实验步骤④所得沉淀是否洗净的方法是:取最后一次洗涤液少量,
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com