
下列说法正确的是()
A. 可利用过滤的方法区别溶液和胶体
B. 制备Fe(OH)3胶体通常是将Fe(OH)3固体溶于沸水
C. 直径介于1nm~100nm之间的微粒称为胶体
D. 电泳现象证明胶体粒子是带电的
考点: 胶体的重要性质.
专题: 溶液和胶体专题.
分析: A、从溶液和胶体透过滤纸分析判断;
B、从实验室制备胶体 的方法和步骤分析判断;
C、从胶体是由分散质和分散剂组成的分析;
D、电泳现象是分散质微粒向电极移动发生的现象;
解答: 解:A、溶液和胶体都能透过滤纸,故A错误;
B、氢氧化铁胶体制备是把饱和氯化铁溶液滴入沸水中加热至红褐色,故B错误;
C、直径介于1nm~100nm之间的微粒为胶体分散质,不是胶体,故C错误;
D、胶体分散质可以吸附带的离子,通电时会移向某一个电极,证明胶粒带电荷,故D正确;
故选D.
点评: 本题考查了胶体的组成、性质、制备等知识的应用,主要是电泳性质的实质.


科目:高中化学 来源: 题型:
如图是向20.00mL盐酸中逐渐滴入NaOH溶液时,溶液pH值变化的图象,根据图象分析,下列结论中不正确的是( )
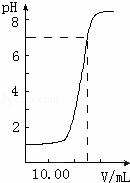
|
| A. | 盐酸起始浓度为0.1mol•L﹣1 |
|
| B. | NaOH溶液浓度为0.08mol•L﹣1 |
|
| C. | 滴入碱量为20mL时,向混合溶液中滴入2滴甲基橙试液,溶液显橙色 |
|
| D. | 滴到中和点时,耗NaOH物质的量为0.002mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是()
A. 含有共价键的化合物一定是共价化合物
B. 在共价化合物中一定含有共价键
C. 含有离子键的化合物一定是离子化合物
D. 双原子单质分子中的共价健一定是非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子能在指定溶液中大量共存的一组是()
A. 在稀盐酸中:Ba2+、CO32﹣、Zn2+
B. 在氢氧化钠溶液中:H+、Mg2+、Cl﹣
C. 在硫酸铵溶液中:Na+、K+、OH﹣
D. 在氯化钠溶液中:K+、Ca2+、N03﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
安全是顺利进行实验及避免伤害的保障.下列实验操作正确且不是从实验安全角度考虑的是()
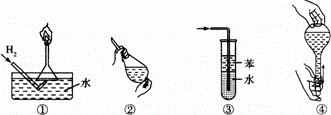
A. 操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B. 操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
C. 操作③:吸收氨气或氯化氢气体并防止倒吸
D. 操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
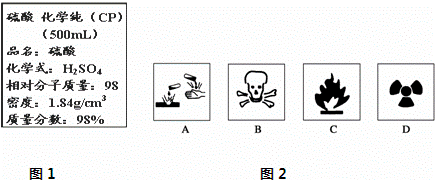
Ⅰ.现欲用该浓硫酸配制成1mol/L的稀硫酸.现实验室仅需要这种稀硫酸220mL.试回答下列问题:
(1)用量筒量取该浓硫酸 mL.
(2)配制时,必须使用的仪器除量筒、烧杯外,还缺少的仪器是 .
(3)若在稀释过程中,浓硫酸不慎沾在手上,处理方法为 .
(4)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是BCF.
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中.
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,俯视容量瓶刻度线
Ⅱ.
(1)在盛放浓硫酸的试剂瓶的标签上应印有图2警示标志中的A.
(2)若将该浓硫酸与等质量的水混合,则所得溶液中溶质物质的量浓度 9.2mol/L(填>、<、=)
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程能量变化如图所示,下列说法正确的是()
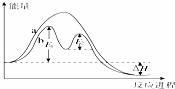
A. 反应过程a有催化剂参与
B. 该反应为放热反应,热效应不等于△H
C. 改变催化剂,可改变该反应的活化能
D. 有催化剂条件下,反应的活化能等于E1+E2
查看答案和解析>>
科目:高中化学 来源: 题型:
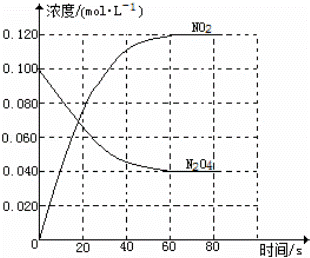
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)⇌2NO2(g),随温度的升高,混合气体的颜色变深.
回答下列问题:
(1)反应的△H 0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为 mol•L﹣1•s﹣1;反应的平衡常数K1为 .
(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol•L﹣1•s﹣1的平均速率降低,经10s又达到平衡.
①T 100℃(填“大于”或“小于”),判断理由是 .
②列式计算温度T时反应的平衡常数K2 .
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向 (填“正反应”或“逆反应”)方向移动,判断理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某KOH样品中含水7.62%,含K2CO32.23%,含KOH90%.现将1.00g样品加入46.00mL1.00mol/L的盐酸中,过量的酸用1.070mol/LKOH溶液刚好中和.蒸发溶液,蒸发到无水时,可得到固体的质量约为( )
|
| A. | 3.00g | B. | 3.43g | C. | 4.50g | D. | 无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com