
| A. | 铜片是负极 | B. | 氢离子在铜片表面被还原 | ||
| C. | 电流从锌片经导线流向铜片 | D. | 铜片质量逐渐减少 |
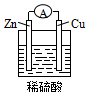
分析 该原电池中,较活泼的金属锌作负极,负极上失电子生成锌离子进入溶液;较不活泼的金属铜作正极,正极上氢离子得电子生成氢气;电子从负极沿导线流向正极,电流流向和电子流向相反,以此解答该题.
解答 解:A.较活泼的金属锌作负极,较不活泼的金属铜作正极,故A错误;
B.铜是正极,正极上氢离子得电子发生还原反应生成氢气,所以氢离子在铜表面被还原,故B正确;
C.电子从负极沿导线流向正极,所以电子从锌片经导线流向铜片,而电流从正极流向负极,故C错误;
D.负极锌失电子生成锌离子进入溶液,所以负极锌质量逐渐减小,正极氢离子在铜表面被还原成氢气,正极铜的质量不变,故D错误;
故选B.
点评 本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,难度不大,注意把握原电池的工作原理.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
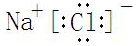 ,反应中被氧化的物质是Fe(OH)3(写化学式).
,反应中被氧化的物质是Fe(OH)3(写化学式).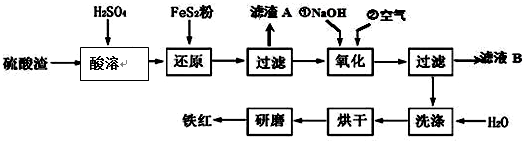
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀盐酸反应 | B. | 灼热的炭与水蒸气的反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 甲烷在氧气中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L氘(D2)气体,含有中子数为2NA | |
| B. | 1.6gNH2-离子所含电子数为NA | |
| C. | 4g氦气所含分子数为0.5NA | |
| D. | NA个SO3分子在标准状况下的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 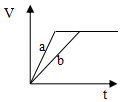 | B. | 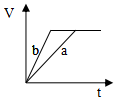 | C. | 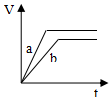 | D. | 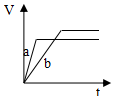 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
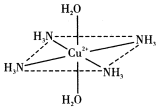 往硫酸铜水溶液中加入氨水,首先生成难溶物,继续加氨水,难溶物溶解,而且所得溶液的颜色比原来明显加深,得到了一种含2+的溶液,此离子的立体结构如图所示(4个NH3与Cu2+共面,跟H2O-Cu2+-H2O轴线垂直).请回答以下问题:
往硫酸铜水溶液中加入氨水,首先生成难溶物,继续加氨水,难溶物溶解,而且所得溶液的颜色比原来明显加深,得到了一种含2+的溶液,此离子的立体结构如图所示(4个NH3与Cu2+共面,跟H2O-Cu2+-H2O轴线垂直).请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子云中的每个小黑点代表一个电子 | |
| B. | σ键采用“肩并肩”的重叠方式 | |
| C. | 含有配位键的化合物就叫配合物 | |
| D. | 血红素、叶绿素、维生素B12都是配合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2F2+2H2O═4HF+O2 | B. | Cl2+H2O═HClO+HCl | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | CO+H2O$\frac{\underline{\;高温\;}}{\;}$CO2+H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com