
分析 (1)据c=$\frac{n}{v}$进行计算;
(2)碳酸钠、碳酸氢钠恰好与盐酸完全反应生成氯化钠与二氧化碳,根据生成二氧化碳的体积,由碳元素守恒可知碳酸钠、碳酸氢总物质的量,再结合二者总质量列方程计算解答.
解答 解:(1)n(HCl)=$\frac{7.84L}{22.4L/mol}$=0.35mol,c(HCl)=$\frac{0.35mol}{0.35L}$=1mol/L,
故答案为:1;
(2)碳酸钠、碳酸氢钠恰好与盐酸完全反应生成氯化钠与二氧化碳,设Na2CO3、NaHCO3的物质的量分别为xmol、ymol,则:
由碳元素守恒,可得:x+y=0.2①,
由Na2CO3、NaHCO3的总质量可得:106x+84y=17.9②,
联立①②方程,解得x=0.05,y=0.15,
故m(Na2CO3=0.05mol×106g/mol=5.3g,
故答案为:5.3.
点评 本题考查混合物有关计算、物质的量浓度计算,难度不大,有利于基础知识的巩固.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
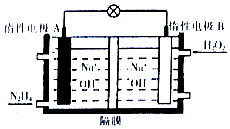 肼(N2H4)是一种高能燃料,在工业生产中用途广泛.
肼(N2H4)是一种高能燃料,在工业生产中用途广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓度均为0.1mol•L-1的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-) | |
| B. | pH相同的盐酸和硫酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH相等,则m>n | |
| C. | 常温下,0.1mol•L-1某一元酸HA在水中有0.1%发生电离,则该温度下HA的电离常数约为10-7 | |
| D. | 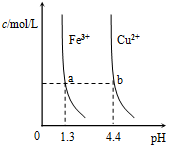 某温度下,Fe(OH)3,Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图.由图可知:Ksp[Fe(OH)3]<K[Cu(OH)2] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验次数 | 混合物的质量/g | 所加Ba(OH)2溶液的体积/L | 测得沉淀的质量/g |
| 1 | 1.716 | 0.5 | 2.758 |
| 2 | 3.432 | 0.5 | |
| 3 | 5.148 | 0.5 | 8.274 |
| 4 | 6.864 | 0.5 | 11.032 |
| 5 | 8.580 | 0.5 | 11.032 |
| 6 | 10.296 | 0.5 | 11.032 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该合金中铝与镁的物质的量之比是2:1 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0mol/L | |
| C. | NO2和NO的混合气体中,NO的体积分数是20% | |
| D. | 得到19.4g沉淀时,加入NaOH溶液的体积是300mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁和铁 | B. | 钠和铁 | C. | 锌和铜 | D. | 铁和铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com