
【题目】可利用如下反应将二氧化碳转化为甲烷:![]()
![]() kJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂
kJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂![]() Ⅰ、Ⅱ
Ⅰ、Ⅱ![]() 作用下,体积为
作用下,体积为![]() 的密闭容器中,
的密闭容器中,![]() 随光照时间的变化曲线。下列说法正确的是
随光照时间的变化曲线。下列说法正确的是

A.![]() 内,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好
内,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好
B.![]() 内,
内,![]() mol/(L·h)
mol/(L·h)
C.a点时,![]() 的转化率相等
的转化率相等
D.反应开始后的![]() 内,第Ⅰ种催化剂的作用下,反应吸收的热量多
内,第Ⅰ种催化剂的作用下,反应吸收的热量多
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】钨是我国丰产元素。科研专家经过长期勘测评审,于2016年元月确认江西省浮梁县存在着世界上最大的钨矿。从而进一步确立了江西省“世界钨都”的地位。自然界中钨有部分是以钨(+6价)酸盐的形式存在。黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),含有SiO2、Al2O3等杂质。现用黑钨矿制备金属钨的流程图如图:
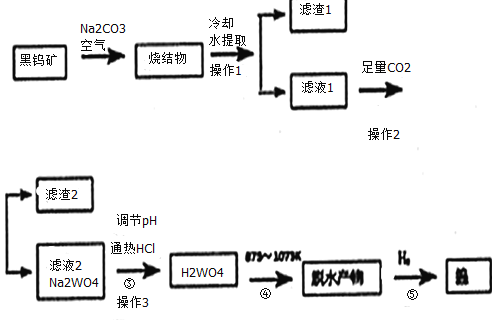
说明:a:反应①是在高温熔融下进行的,烧结物成分为:Fe2O3、Mn2O4、NaAlO2、Na2SiO3、Na2WO4
b:生成Fe2O3的反应为:4FeWO4+4Na2CO3+O2=4Na2WO4+4CO2+2Fe2O3
c:在pH值3.0~4.4的热溶液中,用盐酸沉淀出钨酸与杂质分离,灼烧后即为三氧化钨
回答下列问题:
(1)写出烧结物中生成Na2SiO3的化学反应方程式:__,生成Mn2O4与生成Fe2O3所发生的反应原理相同,请写出生成Mn3O4的化学反应方程式:___。
(2)操作3需要用到玻璃仪器的有:__。
(3)通入足量CO2时发生的离子反应方程式为:___、___。
(4)上述流程最后步骤中钨的制备属于工业冶炼金属的何种方法___。
(5)我国钨化学研究的奠基人顾翼东先生采用另外的反应制得了一种黄色的、非整比的钨的氧化物WO(3-x),这种蓝色氧化钨具有比表面大、易还原得优点。一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在正五价和正六价两种状态的钨,若x的值为0.1,则蓝色氧化钨中这两种价态的钨原子数之比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在容积均为0.5L的两个密闭容器中发生:2A(g)+B(g)2C(g)△H=﹣Q kJ/mol (Q>0),6min后,容器①中反应达平衡,有关数据如下表,下列叙述中正确的是
容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
A | B | C | ||
① | 2 | 1 | 0 | 0.75QkJ |
② | 0.4 | 0.2 | 1.6 | |
A. 0-6min,v(A)=0.25mol/(L·min)
B. ②中达平衡时放出的热量为0.05QkJ
C. 其他条件不变,若容器②保持绝热恒容,则达到平衡时C的体积分数小于2/3
D. 若①达平衡后,再通入1molA与0.5molB,再达平衡时A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的三个容积相同的容器①②③中进行如下反应:3A(g)+B(g) ![]() 2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
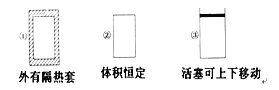
A. ③②①B. ③①②C. ①②③D. ②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的各图中,表示2A(g)+B(g)2C(g)(△H<0)这个可逆反应的正确图象为(注:(C)表示C的质量分数,P表示气体压强,C表示浓度)
A.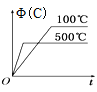 B.
B.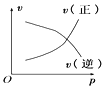 C.
C.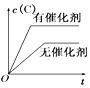 D.
D.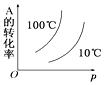
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为![]() 的两个恒容密闭容器中加入足量相同的碳粉,再分别加入
的两个恒容密闭容器中加入足量相同的碳粉,再分别加入![]() 和
和![]() ,在不同温度下反应
,在不同温度下反应![]() 达到平衡,平衡时
达到平衡,平衡时![]() 的物质的量浓度
的物质的量浓度![]() 随温度的变化如图所示
随温度的变化如图所示![]() 图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上
图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上![]() 。下列说法不正确的是
。下列说法不正确的是![]()
![]()

A.反应![]() 的
的![]()
B.体系的总压强![]() 状态Ⅱ
状态Ⅱ![]() 状态Ⅲ
状态Ⅲ![]()
C.体系中![]() ,状态Ⅱ
,状态Ⅱ![]() ,状态Ⅲ
,状态Ⅲ![]()
D.逆反应速率![]() 状态Ⅰ
状态Ⅰ![]() 状态Ⅲ
状态Ⅲ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 在水中的电离方程式为:
在水中的电离方程式为:![]() 。某温度下,向
。某温度下,向![]() 的蒸馏水中加入
的蒸馏水中加入![]() 晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,正确的是
晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,正确的是
A.该溶液中![]() 浓度为
浓度为![]()
B.由水电离出来的![]() 的浓度是
的浓度是![]()
C.加入的![]() 的物质的量为
的物质的量为![]()
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL1mol/LNH2OH![]() 溶液中加水进行稀释,所得曲线如图所示V表示溶液的体积
溶液中加水进行稀释,所得曲线如图所示V表示溶液的体积![]() ,
,![]() 。下列说法不正确的是
。下列说法不正确的是![]()
![]()

A.![]() 的电离平衡常数Kb的数量级为
的电离平衡常数Kb的数量级为![]()
B.用![]() 的盐酸滴定10ml1mol/LNH2OH溶液至
的盐酸滴定10ml1mol/LNH2OH溶液至![]() ,消耗盐酸体积小于10mL
,消耗盐酸体积小于10mL
C.当溶液稀释至![]() 时,溶液中由水电离出的
时,溶液中由水电离出的![]()
D.![]() 溶液中离子浓度大小关系:
溶液中离子浓度大小关系:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某溶液中有浓度均为0.01 mol·L-1的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知25 ℃时,Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4,Ksp[Cr(OH)3]=7.0×10-31 mol4·L-4,Ksp[Zn(OH)2]=1.0×10-17 mol3·L-3,Ksp[Mg(OH)2]=1.8×10-11 mol3·L-3。当下列离子以氢氧化物的形式开始沉淀时,所需的pH最小的是( )
A.Fe3+B.Cr3+C.Zn2+D.Mg2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com