
【题目】在一密闭容器中加入A和B,随着反应的进行,各物质的物质的量浓度变化如图所示。下列说法不正确的是
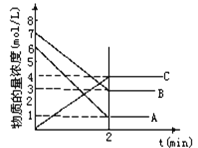
A.该反应的化学方程式为:5A+4B![]() 4C
4C
B.该反应达到平衡时,A、B、C的浓度比为5∶4∶4
C.用B的浓度变化表示2min内的速率为2 mol·L-1·min-1
D.2 min前,正反应速率逐渐减小,逆反应速率逐渐增大
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台化合物。E是一种治疗心绞痛的药物,由葡萄糖为原料合成E的过程如下:
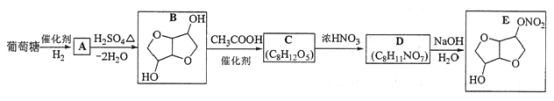
回答下列问题:
(1)葡萄糖的分子式为__________。
(2)A中含有的官能团的名称为__________。
(3)由B到C的反应类型为__________。
(4)C的结构简式为__________。
(5)由D到E的反应方程式为______________。
(6)F是B的同分异构体,7.30 g的F与足量饱和碳酸氢钠反应可释放出2.24 L二氧化碳(标准状况),F的可能结构共有________种(不考虑立体异构),其中核磁共振氢谱为三组峰,峰面积比为3∶1∶1的结构简式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL)。
I.实验步骤:
(1)量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL容量瓶中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴_______________作指示剂。
(3)读取盛装0.1000mol/L NaOH 溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为____________mL。

(4)滴定。当____________时,停止滴定,并记录NaOH溶液的最终读数.再重复滴定3次。
Ⅱ.实验记录
实验数据(mL) 滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理:
(5)某同学在处理数据时计算得:平均消耗的NaOH溶液的体积 V=![]() =15.24mL。指出他的计算的不合理之处:____________________________________。按正确数据处理,可得市售白醋总酸量=____________g/100mL。(结果保留四位有效数字)
=15.24mL。指出他的计算的不合理之处:____________________________________。按正确数据处理,可得市售白醋总酸量=____________g/100mL。(结果保留四位有效数字)
(6)在本实验的滴定过程中,下列操作会使实验结果偏大的是(填写序号)____________。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向0.1mol/L的AlCl3溶液中不断加入NaOH溶液,体系中含铝微粒的分布分数随溶液pH的变化如图所示。下列说法错误的是

A.pH=4的溶液中:c(Al3+)>c[Al(OH)2+]>c[Al(OH)2+]
B.pH=4.5的溶液中:c(H+)+3c(Al3+)+2c[Al(OH)2+]+c[Al(OH)2+]=c(Cl-)+c(OH-)
C.pH=7时,向体系中再加入NaOH溶液,主要发生的离子反应为Al(OH)3+OH-=Al(OH)4-
D.pH=8时,向得到的溶液中通入CO2至饱和,主要发生的离子反应为2Al(OH)4-+CO2=2Al(OH)3↓+CO32-+H2O,CO32-+CO2+H2O=2HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KA1(SO4)2·12H2O]是一种复盐,在造纸等方面应用广泛。采用废易拉罐制备明矾的过程如下图所示。
下列叙述错误的是
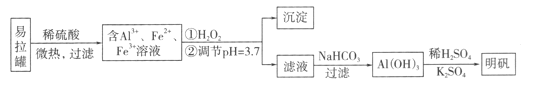
A. 合理处理易拉罐有利于环境保护和资源再利用
B. 从易拉罐中可回收的金属元素有Al、Fe
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用NaHSO4代替NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是

A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①写出二氧化碳的电子式:________________;
②写出赤铁矿石主要成份的化学式:___________________。
③写出氨分子的结构式:__________________。
(2)写出镁在二氧化碳中燃烧的化学方程式__________________________________________________。
(3)写出铜与氯化铁溶液反应的离子方程式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备金属钾的反应:Na+KCl ![]() K+NaCl,有关沸点的数据如下:
K+NaCl,有关沸点的数据如下:
物质 | K | Na | KCl | NaCl |
沸点(°C) | 759 | 883 | 1420 | 1465 |
下列说法不正确的是
A.该反应说明,Na的金属性强于K
B.850°C时,钾蒸气逸出,平衡正向移动,KCl转化率增大
C.升温至900°C,收集金属钾,钾的纯度会降低
D.金属钾中含有杂质钠,可通过真空蒸馏的方法分离提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数的值,下列说法正确的是
A.1mol OH﹣含有的电子数为9NA
B.标准状况下,NO2和N2O4的混合物23g中含有NA个氧原子
C.常温常压下,2.8gN2和2.24L CO所含电子数均为1.4NA
D.标准状况下,22.4 L 乙醇中含有NA个乙醇分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com