
| A. | 原子半径:Z>Y>X | |
| B. | CaY2与水发生氧化还原反应时,CaY2只作氧化剂 | |
| C. | Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 | |
| D. | CaX2、CaY2和CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2 |
分析 X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与S2-的核外电子数相等,3种元素的核外电子数之和为18,Z得到1个电子变成稀有气体的8电子结构,则Z为F元素,则X、Y一定至少有一种位于第2周期,X得到一个电子后均形成稀有气体原子的稳定电子层结构,故X为H元素,Y元素原子核外电子数为18-1-9=8,故Y为O元素,结合选项解答.
解答 解:X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与S2-的核外电子数相等,3种元素的核外电子数之和为18,Z得到1个电子变成稀有气体的8电子结构,则Z为F元素,则X、Y一定至少有一种位于第2周期,X得到一个电子后均形成稀有气体原子的稳定电子层结构,故X为H元素,Y元素原子核外电子数为18-1-9=8,故Y为O元素.
A.X、Y、Z分别是H、O、F,同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径O>F>H,故A错误;
B.CaO2与水反应生成氢氧化钙与氧气,过氧化钙既是氧化剂又是还原剂,故B错误;
C.HF分子之间含有氢键,沸点高于其它同族氢化物的沸点,故C正确;
D.CaH2和CaF2中阴离子分别为H-、F-,阳离子与阴离子的个数比均为1:2,但CaO2中阴离子为O22-,阳离子与阴离子个数比为1:1,故D错误.
故选C.
点评 本题考查结构性质位置关系、氧化还原反应等,难度中等,推断元素是解题关键,B选项中根据过氧化钠与水反应解答.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | 蘸有浓氨水的玻璃棒置于某浓无机酸的试剂瓶口,有大量白烟,说明该酸为盐酸 | |
| B. | 向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振荡后再滴入有机物X,加热至沸后无砖红色沉淀,说明X中不含有醛基 | |
| C. | 向KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去,说明SO2具有还原性 | |
| D. | 往盛有漂粉精溶液的试管中滴加浓硫酸,产生黄绿色气体,说明浓硫酸有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH-CN | B. | CH2═CH-CH═CH2 | C. | 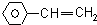 | D. | 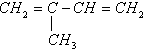 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 将20mL2mol/L的NaOH溶液缓缓地倒入20mL2mol/L的盐酸中,边加边搅拌,测定反应前后溶液温度的变化 | 温度升高 | 释放出的热量就是中和热 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 将一小段镁带和一小块铝分别放在同体积、同浓度的盐酸中 | 都有气泡产生,镁带产生气泡更快 | 镁比铝活泼 |
| D | 将少量氯气通入到NaBr溶液中 | 溶液变成橙红色 | 氯气溶于水呈现橙红色 |
| A. | A | B. | B | C. | C□D.D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
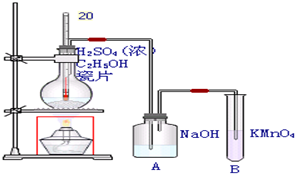
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +45 kJ•mol-1 | B. | +32.7 kJ•mol-1 | C. | -45 kJ•mol-1 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
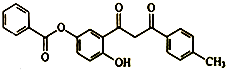
| A. | 分子中含醚键,不含手性碳原子 | |
| B. | 在空气中易被氧化变质 | |
| C. | 能发生取代、加成、消去反应 | |
| D. | 1mol该物质最多能与3mol NaOH溶液发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com