
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,按要求用化学式或化学用语填空,用序号填写不得分。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | |||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为_____________;
(2)地壳中含量最多的非金属元素是_____________;
(3)与水反应最剧烈的金属单质是_____________;
(4)某元素三价阳离子的核外有10个电子,该元素是_____________;
(5)气态氢化物最稳定的化合物是_____________;
(6)①的最高价氧化物的电子式为_____________;
(7)用电子式表示④和⑨形成化合物的过程_____________。
(8)最高价氧化物对应的水化物碱性最强的化合物是_____________;元素的最高价氧化物对应的水化物中具有两性的化合物是_____________;两者反应的离子方程式为_____________。
【答案】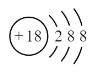 O Na Al HF
O Na Al HF ![]()
![]() NaOH Al(OH)3 Al(OH)3+OH-=AlO2-+2H2O
NaOH Al(OH)3 Al(OH)3+OH-=AlO2-+2H2O
【解析】
由元素在来周期表中位置,可知①为C、②为O、③为F、④为Na、⑤为Mg、⑥为Al、⑦为Si、⑧为P、⑨为Cl、⑩为Ar。根据同周期从左往右元素的非金属性逐渐增强,金属性逐渐减弱,同族从上到下元素的金属性逐渐增强非金属性逐渐减弱可知,在以上金属元素中,金属性最强的是Na,其最高价氧化物的水化物碱性最强,非金属性最强的是F,其氢化物最稳定。
(1)0族元素的化学性质最不活泼,所以在这些元素中,化学性质最不活泼的原子为Ar,其原子结构示意图为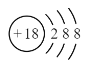 ;
;
(2)地壳中含量最多的非金属元素是O;
(3)与水反应最剧烈的金属单质是Na;
(4)某元素三价阳离子的核外有10个电子,则其原子的核外电子数为13,所以该元素是Al;
(5)F的非金属性最强,其气态氢化物HF最稳定;
(6)①为C,其最高价氧化物为CO2,其电子式为![]() ;
;
(7)用电子式表示的④和⑨形成化合物的过程为:![]() 。
。
(8)最高价氧化物对应的水化物碱性最强的化合物是NaOH;元素的最高价氧化物对应的水化物中具有两性的化合物是Al(OH)3;两者反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:

(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为___;实验过程中,装置B中观察到的现象是______;装置C中有白色沉淀生成,该沉淀是_____(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:______。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为____(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是___。
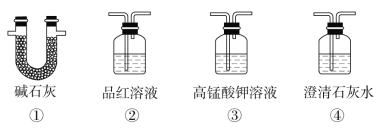
(4)某同学发现实验后期装置A中产生的气体中还含有H2,理由是___________ (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第VIIA族元素的单质及其化合物的用途广泛。完成下列填空:
(1)与氯元素同族的短周期元素的原子核外有_________种不同能量的电子,写出其最外层电子的轨道表示式____________________________。
(2)不能作为溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是______(填序号)。
a.IBr中溴为-1价 b.HBr、HI的酸性
c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)已知:AlF3的熔点为1040℃,AlCl3在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:_____________________________________
(4)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:__________________________________
(5)卤素单质及其化合物在许多性质上都存在递变规律,请从物质结构角度说明下列递变规律的原因。
①熔点按F2、Cl2、Br2、I2的顺序依次升高,原因是__________________________。
②还原性按Cl-、Br-、I-的顺序依次增大,原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 4NH3+5O2 = 4NO+6H2O(g),若反应速率分别用 v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A.v(O2)=![]() v(NH3)B.v(H2O)=
v(NH3)B.v(H2O)= ![]() v(O2)C.v(H2O)=
v(O2)C.v(H2O)=![]() v(NH3)D.v(NO)=
v(NH3)D.v(NO)= ![]() v(O2)
v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型,据此回答下列问题:
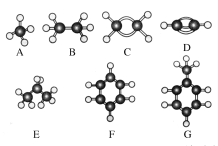
(1)常温下含碳量最高的气态烃是________(填对应字母);
(2)能够发生加成反应的烃有________(填数字)种;
(3)一卤代物种类最多的是________(填对应字母);
(4)写出实验室制取D的化学方程式________________________________;
(5)写出F发生溴代反应的化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产含氯有机物时会产生HCl,利用反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)可实现氯的循环利用。完成下列填空:
2Cl2(g)+2H2O(g)可实现氯的循环利用。完成下列填空:
(1)上述反应若在固定体积的密闭容器中发生,能说明反应已达平衡的是_________(选填序号)。
a.2ν(HCl)正=ν(Cl2)逆 b.体系压强不再改变
c.混合气体密度不变 d.K=![]()
(2)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似。下列有关说法不正确的是___(选填序号)。
a.S2C12分子中有4对共用电子对 b.S2C12分子中没有非极性键
c.S2C12分子中,S为+1价,Cl为-1价 d.S2C12分子中各原子均为8电子稳定结构。
(3)已知X2(g)+H2(g)![]() 2HX(g)+Q(X2表示Cl2、Br2)如图表示上述反应的平衡常数K与温度T的关系。
2HX(g)+Q(X2表示Cl2、Br2)如图表示上述反应的平衡常数K与温度T的关系。
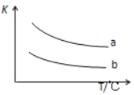
①Q表示X2(g)与H2(g)反应的反应热,Q____0(填“>”、“<”或“=”)。
②写出曲线b表示的平衡常数K的表达式,K=_________________(表达式中写物质的化学式)。
(4)向新制的氯水中加入少量下列物质,能增强溶液漂白能力的是(_______)
A.氯化钙 B.碳酸钙粉末 C.二氧化硫溶液 D.稀硫酸
(5)若向氯化银沉淀中逐渐滴加HBr,会看到白色沉淀逐渐变为淡黄色沉淀现象,请用溶解平衡原理解释此现象____。
(6)已知BBr3与BI3的空间构型是平面三角形结构,则它们是____分子(填极性或非极性),且BBr3的沸点低于BI3,原因是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3CuO+2NH3![]() 3Cu+N2+3H2O。下列判断正确的是
3Cu+N2+3H2O。下列判断正确的是
A.N元素的化合价降低B.NH3被还原
C.消耗0.3 mol CuO转移0.6 NA个电子D.CuO是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
Ⅰ.利用反应:6NO2+8NH3![]() 7N2+12H2O处理
7N2+12H2O处理
Ⅱ.一定条件下NO2与SO2可发生反应:NO2(g)+SO2(g)![]() SO3(g)+NO(g)-Q (Q>0)
SO3(g)+NO(g)-Q (Q>0)
Ⅲ.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
(1)硫离子最外层电子的电子排布式为_____,氨气分子的电子式为______,氨气分子属于______分子(填“极性”或者“非极性”)。
(2)C、O、S这三种元素中属于同周期元素的非金属性由强到弱的顺序为______,能证明其递变规律的事实是_______。
a.最高价氧化物对应水化物的酸性 b.气态氢化物的沸点
c.单质与氢气反应的难易程度 d.其两两组合形成的化合物中元素的化合价
(3)对于Ⅰ中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均速率v(NO2)=_______。
(4)对于Ⅱ中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是______。
a.体系压强保持不变 b.NO2浓度保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
(5)请写出Ⅱ中反应的平衡常数表达式K=_______,如果Ⅱ中反应的平衡常数K值变大,该反应______。
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(6)对于Ⅲ中的反应,CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、1.3×104kPa左右,简述选择此压强的理由:______。
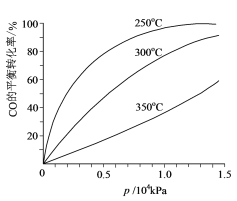
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物(C12H16O2)的性质有如下变化:
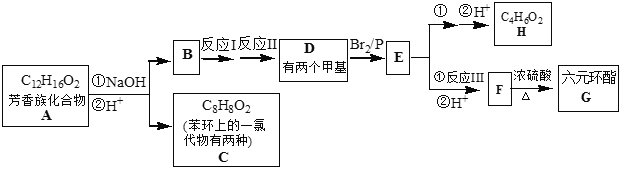
已知: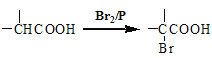
完成下列填空:
(1)E分子中所包含官能团的名称是____。
(2)D的结构简式:____。
(3)写出反应I所需的试剂和条件___;反应Ⅱ和反应Ⅲ的反应类型依次为:____、___;
(4)F生成G的化学方程式:____;
(5)已知M是C的同分异构体。M符合以下条件:
①苯环上有两个取代基(除苯环外无其他的环);②能发生水解反应③苯环上只有两种氢原子。
写出符合条件的M其中任意一种化合物的结构简式:____。
(6)运用中学化学知识及以上信息,写出由E合成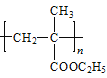 的的合成路线。__
的的合成路线。__
(合成路线常用的表示方式为:A![]() B
B![]() ……目标产物)
……目标产物)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com