
 如图是硫酸试剂瓶标签上的内容:
如图是硫酸试剂瓶标签上的内容:分析 (1)依据C=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度;
(2)需要240ml.4.6mol.L-l的稀硫酸,应选择250mL容量瓶,实际配制250mL溶液,依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸的体积;
(3)依据浓硫酸稀释的正确操作解答;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
(5)①依据定容的正确操作解答;
②不当操作导致实验失败且无法补救的,需要重新配制.
解答 解:(1)浓硫酸的物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L;
故答案为:18.4;
(2)需要240ml.4.6mol.L-l的稀硫酸,应选择250mL容量瓶,实际配制250mL溶液,设需要浓硫酸体积为V,依据溶液稀释过程中溶质的物质的量不变得:V×18.4mol/L=4.6mol/L×250mL,解得V=62.5mL;
故答案为:62.5;
(3)浓硫酸稀释的正确操作为:将量取的浓硫酸沿烧杯内壁缓缓地倒人盛有适量蒸馏水的烧杯中,同时用玻璃棒不断搅拌;
故答案为:将量取的浓硫酸沿烧杯内壁缓缓地倒人盛有适量蒸馏水的烧杯中,同时用玻璃棒不断搅拌;
(4)①用量筒量取浓硫酸时俯视量筒刻度线,导致量取浓硫酸体积偏小,溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
②未经冷却趁热将溶液注入容量瓶中,冷却后溶液体积偏小,溶液浓度偏高;
故答案为:偏高;
③仰视容量瓶刻度线定容,导致溶液体积偏大,溶液浓度偏低;
故答案为:偏低;
④移液时不慎将少量溶液滴在容量瓶外面,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
故答案为:偏低;
(5)①定容的正确操作:向容量瓶中加入蒸馏水,液面离容量瓶颈刻度线下1~2cm时,应改用胶头滴管滴加蒸馏水至液面与刻度线相切;
②加蒸馏水时不慎超过了容量瓶颈刻度线,导致实验失败且无法补救,需要重新配制;
故答案为:①改用胶头滴管滴加蒸馏水至液面与刻度线相切;
②重新配制.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤,熟悉容量瓶构造及使用方法和注意问题是解题关键,题目难度不大.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
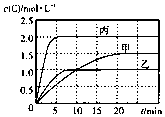 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以表和图表示
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以表和图表示| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5molA 0.5 molB | 1.5 molA 0.5 molB | 6.0 molA 2.0 molB |
| A. | 若平衡时温度不变,改变容器体积平衡不移动 | |
| B. | 由图可知:T1<T2,且该反应为吸热反应 | |
| C. | l0min内甲容器中反应的平均速率v(A)=0.025mol•(L•min)-1 | |
| D. | T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
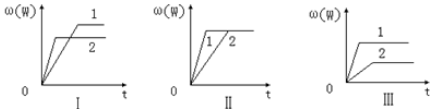
| A. | 图Ⅰ可能是不同压强对反应的影响,且P2>P1,m+n<p | |
| B. | 图Ⅱ可能是不同压强对反应的影响,且P1>P2,m+n=p | |
| C. | 图Ⅲ可能是不同温度对反应的影响,且T1>T2,△H<0 | |
| D. | 若m+n<p,△H>0,则该反应在低温下容易自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ③和④ | C. | ②和③ | D. | 只有③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化学键 | C═O(CO2) | C═O(COS) | C═S | H-S | H-O |
| E(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com