
| A. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| B. | 使用天然气热水器取代电热水器 | |
| C. | 推荐使用手帕,尽量减少使用面纸 | |
| D. | 在建筑、布展、运营过程中应用大规模的太阳能光伏发电系统 |
分析 A.燃煤脱硫技术可以减少二氧化硫的生成;
B.天然气燃烧会产生大气污染物;
C.使用面纸会消耗大量的木材;
D.太阳能属于无污染的可再生能源.
解答 解:A.煤炭中的硫在燃烧时会生成二氧化硫,燃煤脱硫技术可以减少二氧化硫的生成,能防治SO2污染,故A不选;
B.天然气燃烧会产生大气污染物,所以使用天然气热水器取代电热水器会加重空气污染,不符合“绿色城运会”主题,故B选;
C.使用面纸会消耗大量的木材,会使森林减少,使用手帕,尽量减少使用面纸可以保护森林,有利于环境,故C不选;
D.太阳能属于无污染的可再生能源,对环境无害,在建筑、布展、运营过程中应用大规模的太阳能光伏发电系统,可以减少环境污染,故D不选.
故选B.
点评 本题考查了环境保护,题目难度不大,环境污染已影响到人类的生产、生活、身体健康以及人类社会发展,学习时要注意污染的来源、危害、防治措施、变害为利的新工艺.


科目:高中化学 来源: 题型:解答题
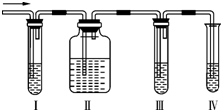 化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了如图所示的实验装置以确认上述混合气体中有C2H4和SO2.回答下列问题:
化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了如图所示的实验装置以确认上述混合气体中有C2H4和SO2.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从合成塔出来的混合气体,其中NH3只占15%,所以合成氨工厂的效率都很低 | |
| B. | 由于氨易液化,N2、H2是循环使用,所以总体来说氨的产率很高 | |
| C. | 合成氨工业的反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动 | |
| D. | 合成氨工厂采用的压强是2×107~5×107Pa,因为在该压强下铁触媒的活性最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强 | B. | 升高温度 | C. | 增大CH4浓度 | D. | 更换高效催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在所有元素中,氟的第一电离能最大 | |
| B. | 氨气的水溶性大于甲烷的水溶性,原因是氨气分子之间能形成氢键 | |
| C. | 元素的金属性越强,其电负性一定越小 | |
| D. | 根据金属元素的逐级电离能数据可大致推断出此元素的最高化合价 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t/s | 0 | 500 | 1000 |
| c(N2O5) mol/L | 5.00 | 3.25 | 2.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应体系的压强,反应速率增大 | |
| B. | 加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量 | |
| C. | 电解熔融的Al2O3和AlCl3均能得到单质铝 | |
| D. | 升高温度,反应的平衡常数将增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
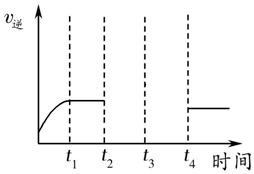 目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究.已知在不同温度下的化学反应平衡常数(K1、K2、K3)如表所示:
目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究.已知在不同温度下的化学反应平衡常数(K1、K2、K3)如表所示:| 化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
| ①2H2(g)+CO(g)?CH3OH(g) | △H1 | K1 | 2.5 | 0.34 | 0.15 |
| ②CO2(g)+H2(g)?CO(g)+H2O(g) | △H2 | K2 | 1.0 | 1.70 | 2.52 |
| ③CO2(g)+3H2(g)?CH3OH(g)+H2O(g) | △H3 | K3 | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com