
【题目】反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

(1)该反应是__反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率_(填“增大”“减小”“不变”),原因是__。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_,E2_,ΔH_(填“增大”“减小”“不变”)。
【答案】放热 减小 升温,平衡逆向移动 减小 减小 不变
【解析】
(1)分析图象中物质能量变化可知:AB反应物能量高于生成物CD,反应是放热反应;
(2) 分析图象可知A(g)+B(g)![]() C(g)+D(g)是放热反应;升高温度平衡逆向移动,A的转化率减小;
C(g)+D(g)是放热反应;升高温度平衡逆向移动,A的转化率减小;
(3)催化剂能同等程度地改变正逆反应速率,减小反应的活化能,不会改变反应热。
(1)分析图象中物质能量变化可知AB反应物能量高于生成物CD,反应是放热反应,A(g)+B(g)![]() C(g)+D(g)过程中的能量变化为放热,故答案为:放热;
C(g)+D(g)过程中的能量变化为放热,故答案为:放热;
(2) A(g)+B(g)![]() C(g)+D(g)反应为放热反应,升高温度平衡逆向移动,A的转化率减小,故答案为:减小;升温,平衡逆向移动;
C(g)+D(g)反应为放热反应,升高温度平衡逆向移动,A的转化率减小,故答案为:减小;升温,平衡逆向移动;
(3)其它条件不变在反应体系中加入催化剂,能同等程度地改变正逆反应速率,降低了反应的活化能,反应物和生成物的活化能都会降低,但物质的反应热不变即ΔH不变,故答案为:减小;减小;不变。


科目:高中化学 来源: 题型:
【题目】铁氮化合物(![]() )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某![]() 的制备需铁、氮气、丙酮和乙醇参与。
的制备需铁、氮气、丙酮和乙醇参与。
(1)![]() 基态核外电子排布式为_______。
基态核外电子排布式为_______。
(2)丙酮(![]() )分子中碳原子轨道的杂化类型是_______,1mol丙酮分子中含有σ键的数目为______________。
)分子中碳原子轨道的杂化类型是_______,1mol丙酮分子中含有σ键的数目为______________。
(3)C、H、O三种元素的电负性由小到大的顺序为_____。
(4)乙醇的沸点高于丙酮,这是因为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铜阳极泥(主要成分是Cu2Te,含Ag、Au等杂质)为原料提取碲并回收金属,其工艺流程如下:
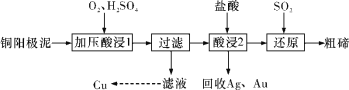
已知:TeO2是两性氧化物,微溶于水,易溶于较浓的强酸和强碱。下列说法错误的是
A.“加压酸浸1”过程中将碲元素转化成TeO2,应严格控制溶液的pH值
B.“酸浸2”过程中温度不能过高,否则会使碲的浸出率降低
C.从Ag和Au中分离出Au,应该向回收的Ag和Au中加入稀氨水
D.“还原”反应中发生的离子方程式为:TeO2+2SO2+2H2O=Te+2SO42-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒容的条件下对于N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为
2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为
A.断开一个N≡N键的同时有6个N—H键生成
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.N2、H2、NH3分子数之比为1∶3∶2的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

已知:①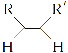
![]() RCHO+R′CHO
RCHO+R′CHO
②RCHO+R′CH2CHO![]()
![]() +H2O
+H2O
③![]()
请回答下列问题:
(1)芳香族化合物B的名称为________,1molB最多能与_____molH2加成,其加成产物等效氢共有_______种。
(2)由E生成F的反应类型为________,F分子中所含官能团的名称是_______。
(3)X的结构简式为________。
(4)写出D生成E的第①步反应的化学方程式______。
(5)G与乙醇发生酯化反应生成化合物Y,Y有多种同分异构体,其中符合下列条件的同分异构体有________种,写出其中任意一种的结构简式____。
①分子中含有苯环,且能与饱和碳酸氢钠溶液反应放出CO2;②其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1。
(6)根据题目所给信息,设计由乙醛和苯甲醛制备![]() 的合成路线(无机试剂任选)______。
的合成路线(无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,装置(I)是一种可充电电池,装置(Ⅱ)为惰性电极的电解池。下列说法正确的是

A. 闭合开关K时,电极B为负极,且电极反应式为:2Brˉ-2eˉ=Br2
B. 装置(I)放电时,总反应为:2Na2S2+Br2=Na2S4+2NaBr
C. 装置(I)充电时,Na+从左到右通过阳离子交换膜
D. 该装置电路中有0.1moleˉ通过时,电极Ⅹ上析出3.2gCu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,H2CO3的Ka1=4.2×10-7,Ka2=5.0×10-11。常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入40mL0.1mol/L'HCl溶液,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
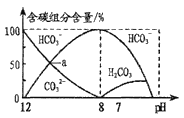
下列说法正确的是
A. 在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
B. a点时:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C. 当pH=7时,溶液中c(Na+)=c(HCO3-)+2c(CO32-)
D. 当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知二甲苯的结构: 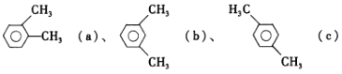 ,下列说法正确的是
,下列说法正确的是
A.a的同分异构体只有b和c两种
B.在三种二甲苯中,b的一氯代物种数最多
C.a、b、c 均能使酸性 KMnO4溶液、溴水发生化学反应而褪色
D.a、b、c 中只有c 的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水垢中含有的 CaSO4,可先用 Na2CO3 溶液处理,使之转化为疏松、易溶于酸的 CaCO3。某化学兴 趣小组用某浓度的 Na2CO3 溶液处理一定量的 CaSO4 固体,测得所加 Na2CO3 溶液体积与溶液中-lgc(CO32-) 的关系如图所示,已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是
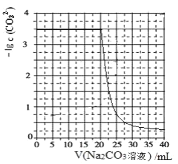
A.曲线上各点的溶液满足关系式:c(Ca2+)×c(SO42-)=Ksp(CaSO4)
B.CaSO4(s)+CO32-(aq) ![]() CaCO3(s)+SO42-(aq) K=3×103
CaCO3(s)+SO42-(aq) K=3×103
C.该Na2CO3溶液的浓度为1.5mol·L-1
D.相同条件下,若将Na2CO3溶液的浓度改为原浓度的2倍,则上图曲线整体向上平移1个单位即可
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com