
| A. | 22.4 L Cl2完全溶于氢氧化钠溶液时,转移电子数为NA | |
| B. | 常温下,1 L pH=1的H2SO4溶液中含有的H+的数目为0.2NA | |
| C. | 标准状况下,2.24 L NH3中含有共价键的数目为0.3NA | |
| D. | 常温下,22.4 L NO2和N2O4的混合气体中含有NA个氧原子 |
分析 A、气体体积,温度压强不知不能计算物质的量;
B、依据溶液浓度和氢离子浓度计算分析;
C、标准状况下,2.24 L NH3物质的量为0.1mol,结合氨气分子式计算共价键数;
D、常温下,22.4 L NO2和N2O4的混合气体物质的量不是1mol.
解答 解:A、气体体积,温度压强不知不能计算物质的量,故A错误;
B、1 L pH=1的H2SO4溶液中含有的H+的数目=1L×0.1mol/L×NA=0.1NA,故B错误;
C、标准状况下,2.24 L NH3物质的量为0.1mol,结合氨气分子式计算共价键数=0.3NA,故C正确;
D、常温下,22.4 L NO2和N2O4的混合气体物质的量不是1mol,22.4 L NO2和N2O4的混合气体中含有氧原子不是NA个,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积的体积应用分析,氧化还原反应电子转移的计算,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 步骤①的化学方程式为:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| B. | 步骤①②③中每生成或反应1mol Si,转移4mol电子 | |
| C. | 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应 | |
| D. | SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
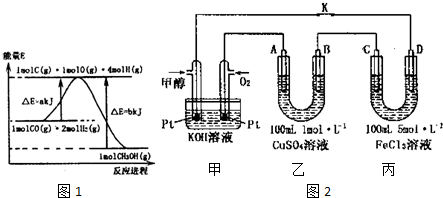
| 温度\时间 | 10min | 20min | 30min | 40min | 50min | 60min |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
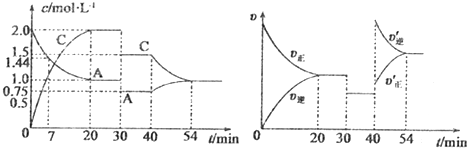
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
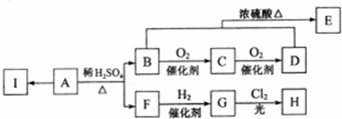
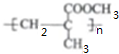 .
.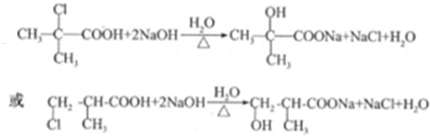 (任写一个)
(任写一个)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 篮球架的表面喷涂油漆,主要是为了美观 | |
| B. | 回收金属饮料罐,只是为了减少环境污染 | |
| C. | 银的导电性比铜好,所以常用银作电线而不用铜 | |
| D. | 不锈钢抗腐蚀性好,常用于制医疗器械、炊具等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入l0%的NaOH溶液,得到沉淀的质量记录如下:
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入l0%的NaOH溶液,得到沉淀的质量记录如下:| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
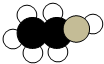 如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质的说法正确的是( )
如图是某有机物分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子.关于该物质的说法正确的是( )| A. | 能使紫色石蕊变红 | B. | 能与Na2CO3反应 | ||
| C. | 能发生酯化反应 | D. | 不能发生氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com