
| A. | 常温常压下,48gO3含有的氧分子数为3NA | |
| B. | 标准状况下,1.8g的水中含有的氧原子数为0.1NA | |
| C. | 22.4 L O2中含有的氧气分子数约为6.02×1023 | |
| D. | 1mol O2氧气分子所占的体积数约为22.4 L |
分析 A、根据分子个数N=$\frac{m}{M}{N}_{A}$来分析;
B、求出水的物质的量,然后根据1mol水中含1mol氧原子来分析;
C、氧气所处的状态不明确;
D、气体所处的状态不明确.
解答 解:A、含有的分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{48g}{48g/mol}{N}_{A}$=NA,故A错误;
B、1.8g水的物质的量n=$\frac{1.8g}{18g/mol}$=0.1mol,而1mol水中含1mol氧原子,故0.1mol水中含0.1mol氧原子即0.1NA个,故B正确;
C、氧气所处的状态不明确,不一定是标况,故22.4L氧气的物质的量不一定是1mol,则含有的氧分子个数不一定是NA个,故C错误;
D、气体所处的状态不明确,不一定是标况,故1mol氧气的体积不一定是22.4L,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:解答题
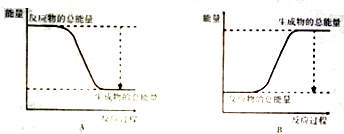
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10%的H2SO4溶液 | B. | NaCl | ||
| C. | 碱石灰(固体,含NaOH,CaO) | D. | Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
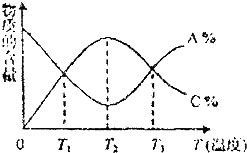
| A. | 该反应在T1、T3温度时达到过化学平衡 | |
| B. | 该反应的正反应是吸热反应 | |
| C. | 该反应在T2温度时达到过化学平衡 | |
| D. | 升高温度,平衡会向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电反应的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列关于此电池说法正确的是( )
如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电反应的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列关于此电池说法正确的是( )| A. | 充电过程中,当0.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子 | |
| B. | 电池放电时,负极反应为:3NaBr一2e-═NaBr3+2Na+ | |
| C. | 充电过程中钠离子从右到左通过离子交换膜 | |
| D. | 放电过程中钠离子从左到右通过离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中Cu2+浓度增大 | B. | 溶液中Cu2+数目减少 | ||
| C. | 该硫酸铜晶体体积增大 | D. | 溶液的蓝色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
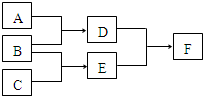 单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系(可能有部分生成物未标出),请回答下列问题:
单质A、B、C和化合物D、E、F,在一定条件下有如图的转化关系(可能有部分生成物未标出),请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com