
| A�� | 2 mol H2O��Ħ��������1mol H2O��Ħ������ | |
| B�� | 200 mL 1 mol•L-1�Ȼ�����Һ��c��Cl-����100 mL 2 mol•L-1�Ȼ�����Һ��c��Cl-�� | |
| C�� | 64 g������������ԭ�����ͱ�״����22.4 Lһ����̼����ԭ���� | |
| D�� | 20% NaOH��Һ��NaOH�����ʵ���Ũ�Ⱥ�10% NaOH��Һ��NaOH�����ʵ���Ũ�� |
���� A��ˮ��Ħ��������ȣ�
B��1mol/L�Ȼ�����Һ��c��Cl-��=1mol/L��2mol/L�Ȼ�����Һ��c��Cl-��=2mol/L��
C������n=$\frac{m}{M}$��������������ʵ�����������ԭ�����ʵ���Ϊ���������2��������n=$\frac{V}{{V}_{m}}$����CO���ʵ���������Oԭ�����ʵ�������CO���ʵ�����
D����Һ���ʵ���Ũ��c=$\frac{1000�Ѧ�}{M}$��20%NaOH��Һ�ܶȴ���10%��NaOH��Һ�ܶȣ�
��� �⣺A��2molˮ��������1molˮ��������2������ˮ��Ħ������Ϊ��ֵ��18g/mol����A����
B��1mol/L�Ȼ�����Һ��c��Cl-��=1mol/L��2mol/L�Ȼ�����Һ��c��Cl-��=2mol/L��������Ũ�Ⱥ�����ǰ�ߵ�2������B����
C�������������ʵ���Ϊ$\frac{64g}{64g/mol}$=1mol��������ԭ�����ʵ���Ϊ2mol�������22.4LCO���ʵ���Ϊ1mol������Oԭ�����ʵ���Ϊ1mol��ǰ���Ǻ��ߵ�2������C��ȷ��
D����Һ���ʵ���Ũ��c=$\frac{1000�Ѧ�}{M}$��20%NaOH��Һ�ܶȴ���10%��NaOH��Һ�ܶȣ���ǰ�����ʵ���Ũ�ȴ��ں��ߵ�2������D����
��ѡC��
���� ���⿼�����ʵ����йؼ��㡢Ħ�����������ʵ���Ũ�ȵȣ��Ѷ��еȣ�ע�������������ʵ���Ũ������������֮��Ĺ�ϵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϵ��ѹǿ���ٸı� | |
| B�� | ��ϵ���¶Ȳ��ٸı� | |
| C�� | ����1molN2��ͬʱ��������3molH2 | |
| D�� | ��Ӧ���ĵ�N2��H2�������NH3�����ʦԣ�N2�����ԣ�H2�����ԣ�NH3���T1��3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
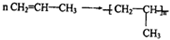
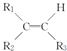 $\stackrel{KMnO_{4}��H+��}{��}$
$\stackrel{KMnO_{4}��H+��}{��}$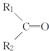 +R3-COOH��
+R3-COOH��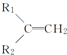 $\stackrel{KMnO_{4}��H+��}{��}$
$\stackrel{KMnO_{4}��H+��}{��}$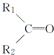 +CO2
+CO2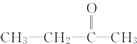 �������ϩ���Ľṹ��ʽ��CH2=C��CH3��C2H5��
�������ϩ���Ľṹ��ʽ��CH2=C��CH3��C2H5���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol �κ�����������Լ��22.4L | |
| B�� | lmolH2��O2�Ļ�����壬�ڱ�״���µ����Ҳ��22.4L | |
| C�� | lmol H2��̬���ʣ������Ϊ22.4L ʱ��������һ�����ڱ�״ | |
| D�� | 2mol �������ԼΪ44.8L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 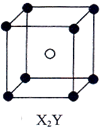 | B�� | 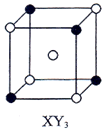 | C�� | 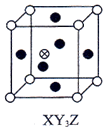 | D�� | 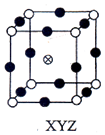 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5 L 1 mol•L-1 MgCl2��Һ�к��е�Cl-��ĿΪ0.5��6.02��1023 | |
| B�� | ��0�桢101kPaʱ��22.4 L H2�к���6.02��1023����ԭ�� | |
| C�� | 14 g N2�к���6.02��1023��ԭ�� | |
| D�� | 6.02��1023��CO2������0.5 mol CH4��������Ϊ7��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol H2Լ����6.02��1023������� | |
| B�� | 1 mol H2O������Ϊ18 g | |
| C�� | 1 mol O2�����Ϊ22.4 L | |
| D�� | 1L 1 mol/L NaCl��Һ�к�1 molNa+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Al��Ӧ������������Һ��K+��Na+��SO42-��HCO3- | |
| B�� | ��Һ��c��H+��/c��OH-��=1014��Fe2+��Na+��SO42-��NO3- | |
| C�� | PH=12����Һ��Na+��K+��AlO2-��Cl- | |
| D�� | ��Һ��ˮ�������H+��OH-����c��H+��•c��OH-��=10-26��NH4+��Mg2+��SO42-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | p�����������ڡ���B�� | B�� | ds�����������ڡ���B�� | ||
| C�� | d�����������ڡ���B�� | D�� | ds�����������ڡ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com