
| 选项 | 实验操作 | 现 象 | 结 论 |
| A | 向亚硫酸钠试样中滴入盐酸酸化的Ba(ClO)2溶液 | 生成白色沉淀 | 试样己氧化变质 |
| B | 向Co2O3中滴入浓盐酸 | 产生黄绿色气体 | 氧化性:Co2O3>Cl2 |
| C | 向待测液中依次滴入氯水和KSCN溶液 | 溶液变为红色 | 待测溶液中含有Fe2+ |
| D | 向Na2SO4和Na2CO3混合溶液中滴入AgNO3溶液 | 产生白色沉淀 | Ksp(Ag2SO4)<Ksp(Ag2CO3) |
| A. | A | B. | B | C. | C | D. | D |
分析 A.滴入盐酸酸化的Ba(ClO)2溶液,HClO可氧化亚硫酸钠;
B.Co2O3中滴入浓盐酸,发生氧化还原反应生成氯气;
C.滴入氯水可氧化亚铁离子;
D.二者均与硝酸银反应生成白色沉淀.
解答 解:A.滴入盐酸酸化的Ba(ClO)2溶液,HClO可氧化亚硫酸钠,应溶于水,加氯化钡检验是否变质,故A错误;
B.Co2O3中滴入浓盐酸,发生氧化还原反应生成氯气,则氧化性:Co2O3>Cl2,故B正确;
C.滴入氯水可氧化亚铁离子,应先加KSCN溶液无现象,再加氯水变血红色检验,故C错误;
D.二者均与硝酸银反应生成白色沉淀,不能比较Ksp,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、离子检验、Ksp比较为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:选择题
| 实验编号 | 温度/℃ | 平衡常数/mol-1•L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | ||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
| A. | 实验1在前6min的平均反应速率υ(SO2)=0.2 mol•L-1•min-1 | |
| B. | T1、T2的关系:T1>T2 | |
| C. | K1、K2的关系:K2>K1 | |
| D. | x=1.6,y=0.2,t<6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 用浸有酸性高锰酸钾溶液的硅藻土作水果保鲜剂 | 酸性高锰酸钾溶液能氧化水果释放的催熟剂乙烯 |
| B | 用氢氟酸蚀刻玻璃 | SiO2是碱性氧化物,能溶于酸 |
| C | 过氧化钠作呼吸面具中的供氧剂 | 过氧化钠是强氧化剂,能氧化二氧化碳 |
| D | Al(OH)3用作塑料的阻燃剂 | Al(OH)3受热熔化放出大量的热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硬脂酸甘油酯在酸性条件下的水解反应叫皂化反应 | |
| B. | 淀粉和纤维素两者不是互为同分异构体,在一定条件下水解均可得到葡萄糖 | |
| C. | 蛋白质遇甲醛可发生变性而凝聚,遇伤口流血时,可在伤口处滴甲醛水溶液来止血 | |
| D. | 在乙酸与乙醛的混合溶液中加入银氨溶液,水浴加热,可观察到银镜现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物的熔沸点都比较低 | |
| B. | 氢的三种核素可组成6种水分子 | |
| C. | H2O分子比H2S分子稳定的原因,是H2O分子间存在氢键 | |
| D. | SiO2和CaCO3在高温下反应生成CO2气体,说明硅酸的酸性比碳酸强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入Al能放出H2的溶液:K+、Cu2+、NO3-、SO42- | |
| B. | 某无色透明溶液:Fe2+、ClO-、SiO32-、Na + | |
| C. | 加入(NH4)2CO3后加热,有气体产生的溶液:Na+、K+、NO3-、Cl- | |
| D. | 0.1mol/LNaHCO3溶液:Na+、A13+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 苯甲醛 | 苯甲酸 | 苯甲醇 | |
| 沸点/℃ | 178.1 | 249.2 | 205.4 |
| 熔点/℃ | -26 | 121.7 | -15.3 |
| 溶解性 ( 常温 ) | 微溶于水,易溶于有机溶剂 | ||
| A. | 苯甲醛既发生了氧化反应,又发生了还原反应 | |
| B. | 可用银氨溶液判断反应是否完全 | |
| C. | 反应后的溶液先用分液法分离出有机层,再用蒸馏法分离出苯甲醇 | |
| D. | 反应后的溶液中加酸、酸化后,用过滤法分离出苯甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
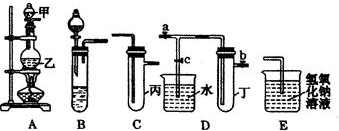
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将所得氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 向所得氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生一种酸性强于碳酸的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1 mol•L-1CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 在0.l mol•L-1的稀硫酸加水稀释的过程中,c(H+):c(SO42-)始终为2:1 | |
| C. | 向10 mL浓度为0.l mol•L-1CH3COOH溶液中滴加相同浓度的氨水至中性,在滴加过程中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$逐渐减小 | |
| D. | 在含0.1mol NaHSO4溶液中:c(H+)<c(SO42-)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com