
| A、③⑤ | B、①③ | C、仅有③ | D、②④ |


 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
| A、能使pH试纸变红的溶液中:CO32-、Ba2+、Cl-、Na+ | ||
| B、由水电离产生的c(OH-)=1×10-10 mol/L的溶液中:NO3-、Mg2+、SO42-、Fe2+ | ||
C、在
| ||
| D、无色透明溶液中:Al3+、HCO3-、Cl-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、⑥②③⑤⑦④① |
| B、①④⑦③⑤②⑥ |
| C、①④⑤③⑦②⑥ |
| D、①④⑦⑤③②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、① | B、② | C、④ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
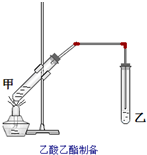 如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁有良好的导热性,常用来制作炊具 |
| B、铜的化学性质不活泼,在潮湿的空气中不会生锈 |
| C、废旧电池中汞的回收可减少对环境的污染 |
| D、铝表面易形成致密的氧化膜可阻止铝进一步被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com