
| A. | 在放电时,正极发生的反应是Pb(s)+SO42-(aq)-2e-═PbSO4(s) | |
| B. | 在放电时,该电池的负极材料是铅板 | |
| C. | 在充电时,电池中硫酸的浓度不断变小 | |
| D. | 在充电时,阳极发生的反应是PbSO4(s)+2e-═Pb(s)+SO42-(aq) |
分析 放电时,该装置是原电池,负极上铅失电子发生氧化反应,正极上二氧化铅得电子发生还原反应,根据电池总反应可知反应消耗硫酸,所以硫酸的浓度减小,结合电极反应式分析判断.
解答 解:A.放电时,该装置是原电池,正极上二氧化铅得电子发生还原反应,则正极发生的反应是PbO2+4H++SO42-+2e-=PbSO4(s)+2H2O,故A错误;
B.放电时,该装置是原电池,负极上铅失电子发生氧化反应,故B正确;
C.放电时,电池反应要消耗硫酸,所以硫酸的浓度减小,故C错误;
D.充电时阳极发生氧化反应,阳极反应为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,故D错误;
故选B.
点评 本题考查了原电池和电解池原理,难点是电极反应式的书写,根据得失电子结合电解质溶液写电极反应式,题目难度不大.


科目:高中化学 来源: 题型:解答题
 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌做负极发生氧化反应 | |
| B. | 供电时的总反应为:Zn+2H+═Zn2++H2↑ | |
| C. | 该装置可实现化学能转化为电能 | |
| D. | 产生1 g H2,消耗锌的质量65 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ②③⑤ | C. | ①③④ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.0 mol | B. | 1.5mol | C. | 1.0mol | D. | 0.75mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物油存放过久,会有一种难闻的“哈喇”味,但不影响食用 | |
| B. | 葡萄糖能发生水解反应 | |
| C. | 淀粉和纤维素水解的最终产物是葡萄糖 | |
| D. | 氨基酸分子中含有氨基和羧基,因此具有两性,但蛋白质没有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示(某些条件和部分产物已略去).下列说法错误的是( )
甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示(某些条件和部分产物已略去).下列说法错误的是( )| A. | 若戊为一种强碱且焰色反应为黄色,则上述反应可能都属于氧化还原反应 | |
| B. | 常温下,若丙为无色气体,戊为红棕色气体,则甲、乙一定是铜和稀硝酸 | |
| C. | 若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲 | |
| D. | 若甲为浓盐酸,乙为MnO2,则戊可能使品红褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化工工业中常用乙苯脱氢的方法制备苯乙烯.
化工工业中常用乙苯脱氢的方法制备苯乙烯.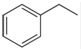 (g)→
(g)→ (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol; (g)+CO(g)+H2O(g) △H=+158.8 kJ/mol
(g)+CO(g)+H2O(g) △H=+158.8 kJ/mol查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com