
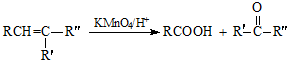
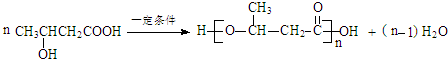 :.
:. .
. .
. .
.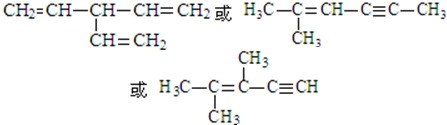 .
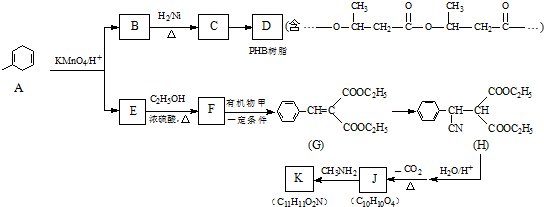
. 分析 由题目信息②可知,A被高锰酸钾溶液氧化生成B、E分别为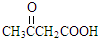 、HOOCCH2COOH中的一种,根据PHB树脂结构简式知,C发生缩聚反应生成PHB,则C结构简式为
、HOOCCH2COOH中的一种,根据PHB树脂结构简式知,C发生缩聚反应生成PHB,则C结构简式为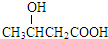 ,B和氢气发生加成反应生成C,则B为
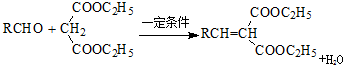
,B和氢气发生加成反应生成C,则B为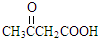 ,故E为HOOCCH2COOH.E与甲醇发生酯化反应生成F,F和甲反应生成G,根据信息③知甲为
,故E为HOOCCH2COOH.E与甲醇发生酯化反应生成F,F和甲反应生成G,根据信息③知甲为 ,F为CH3CH2OOCCH2COOCH2CH3,G与HCN发生加成反应生成H,H发生水解反应、再脱去分子二氧化碳生成J,1mol J最多与2molNaHCO3反应,说明J中含有两个羧基,J和CH3NH2反应生成K,根据分子式知,J发生取代反应生成K,K分子结构中含有一个五元环与一个六元环,J中2个羧基与CH3NH2脱水,2个羧基之间相隔2个碳原子,J结构简式为
,F为CH3CH2OOCCH2COOCH2CH3,G与HCN发生加成反应生成H,H发生水解反应、再脱去分子二氧化碳生成J,1mol J最多与2molNaHCO3反应,说明J中含有两个羧基,J和CH3NH2反应生成K,根据分子式知,J发生取代反应生成K,K分子结构中含有一个五元环与一个六元环,J中2个羧基与CH3NH2脱水,2个羧基之间相隔2个碳原子,J结构简式为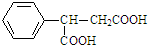 ,K结构简式为
,K结构简式为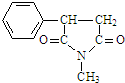 ,据此解答.
,据此解答.
解答 解:由题目信息②可知,A被高锰酸钾溶液氧化生成B、E分别为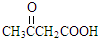 、HOOCCH2COOH中的一种,根据PHB树脂结构简式知,C发生缩聚反应生成PHB,则C结构简式为
、HOOCCH2COOH中的一种,根据PHB树脂结构简式知,C发生缩聚反应生成PHB,则C结构简式为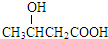 ,B和氢气发生加成反应生成C,则B为
,B和氢气发生加成反应生成C,则B为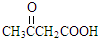 ,故E为HOOCCH2COOH.E与甲醇发生酯化反应生成F,F和甲反应生成G,根据信息③知甲为
,故E为HOOCCH2COOH.E与甲醇发生酯化反应生成F,F和甲反应生成G,根据信息③知甲为 ,F为CH3CH2OOCCH2COOCH2CH3,G与HCN发生加成反应生成H,H发生水解反应、再脱去分子二氧化碳生成J,1mol J最多与2molNaHCO3反应,说明J中含有两个羧基,J和CH3NH2反应生成K,根据分子式知,J发生取代反应生成K,K分子结构中含有一个五元环与一个六元环,J中2个羧基与CH3NH2脱水,2个羧基之间相隔2个碳原子,J结构简式为
,F为CH3CH2OOCCH2COOCH2CH3,G与HCN发生加成反应生成H,H发生水解反应、再脱去分子二氧化碳生成J,1mol J最多与2molNaHCO3反应,说明J中含有两个羧基,J和CH3NH2反应生成K,根据分子式知,J发生取代反应生成K,K分子结构中含有一个五元环与一个六元环,J中2个羧基与CH3NH2脱水,2个羧基之间相隔2个碳原子,J结构简式为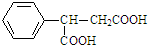 ,K结构简式为
,K结构简式为 .
.
(1)通过以上分析知,B与氢气发生加成反应生成C,也属于还原反应,
故答案为:加成反应(或还原反应);
(2)C结构简式为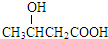 ,C发生缩聚反应生成D,反应方程式为
,C发生缩聚反应生成D,反应方程式为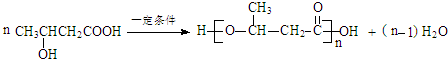 ,
,
故答案为: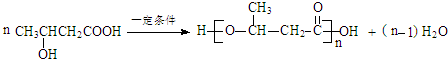 ;
;
(3)通过以上分析知,甲为 ,故答案为:
,故答案为: ;
;
(4)E和乙醇发生酯化反应生成F,反应方程式为: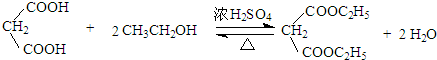 ,
,
故答案为: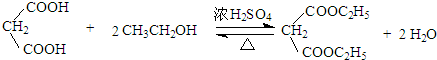 ;
;
(5)J结构简式为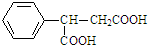 ,K结构简式为
,K结构简式为 ,J发生取代反应生成K,反应方程式为
,J发生取代反应生成K,反应方程式为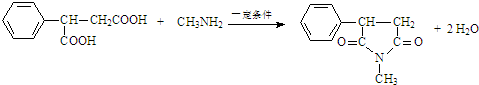 ,
,
故答案为: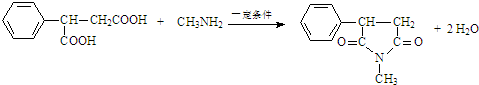 ;
;
(6)A结构简式为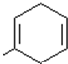 ,S是A的一种同分异构体,分子中没有环状结构,含有含有3个双键,或1个双键、1个三键,S的核磁共振氢谱有三个峰,峰面积之比为6:3:1,则S的结构简式为
,S是A的一种同分异构体,分子中没有环状结构,含有含有3个双键,或1个双键、1个三键,S的核磁共振氢谱有三个峰,峰面积之比为6:3:1,则S的结构简式为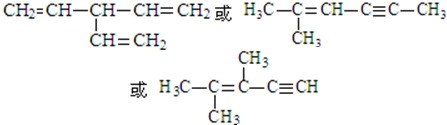 ,
,
故答案为: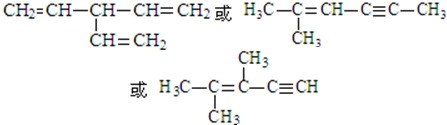 .
.
点评 本题考查有机物推断,需要学生对给予的信息进行利用,侧重考查学生分析推理、知识迁移能力,充分利用流程图中反应条件、物质结构变化结合题给信息进行推断,题目难度中等.


 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:选择题
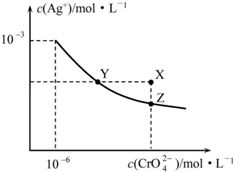
| A. | 在t℃时,Ag2CrO4的Ksp=1×10-9 | |
| B. | X点有Ag2CrO4沉淀生成 | |
| C. | 通过加热蒸发可以使溶液由Y点变到Z点 | |
| D. | 在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点变到X点最终变到Z点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时正极附近溶液的碱性增强 | |
| B. | 充电时锌极与外电源正极相连 | |
| C. | 放电时每转移3 mol电子,正极有1mol K2FeO4被还原 | |
| D. | 充电时阳极反应为:Fe(OH)3-3e-+5OH-═FeO42-+4 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
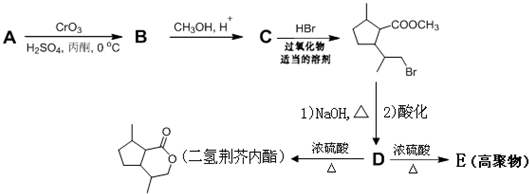
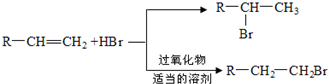
 ,D中含有的官能团的名称羧基、羟基.
,D中含有的官能团的名称羧基、羟基.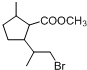 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$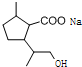 +CH3OH+NaBr.
+CH3OH+NaBr.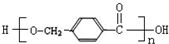 )的路线补全完整
)的路线补全完整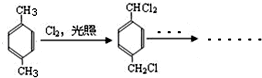
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在涂料中尽量用液态有机物代替水作溶剂,以减少环境污染 | |
| B. | 我国自行研制的“神七”航天服是由新型“连续纤维增韧”材料做成的,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 | |
| C. | 开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 | |
| D. | 醋酸纤维、硝化纤维、合成纤维、光导纤维都可由纤维素在一定条件下制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
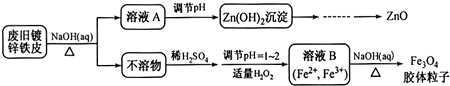
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
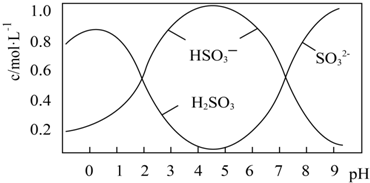
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中加入NaOH溶液 | B. | AlCl3溶液中加入足量的氨水 | ||
| C. | AlCl3溶液中加入石灰水 | D. | Al2O3溶于足量的热水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com