
| A. | 氢氧化钠溶液 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 氯化钠溶液 |
分析 玻璃的成分中含有二氧化硅,二氧化硅是酸性氧化物,能和强碱反应,故强碱性的溶液需要用带橡胶塞的试剂瓶存放,据此分析.
解答 解:A、氢氧化钠呈强碱性,能和二氧化硅反应生成硅酸钠,硅酸钠具有黏性,能把玻璃塞黏住,故A正确.
B、稀盐酸呈酸性,不和二氧化硅反应,所以可以用带玻璃塞的试剂瓶盛放,故B错误.
C、浓硫酸呈酸性,不和二氧化硅反应,所以可以用带玻璃塞的试剂瓶盛放,故C错误.
D、氯化钠溶液显中性,和二氧化硅不反应,故可以用带玻璃塞的试剂瓶盛放,故D错误.
故选A.
点评 本题考查了化学试剂的存在,难度不大,玻璃的成分中含有二氧化硅,二氧化硅能和强碱或氢氟酸反应,所以强碱溶液不能用带玻璃塞的试剂瓶存放,碱式滴定管下端不是玻璃塞是橡胶管.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 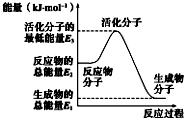 反应②中的能量变化如图所示,则△H2=E1-E3 | |
| B. | N2的燃烧热为180kJ•mol-1 | |
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和 3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和 6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 | |
| D. | 氨的催化氧化反应为 4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=+906 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由强极性键形成的化合物不一定是强电解质 | |
| B. | 强电解质溶液的导电能力一定比弱电解质溶液强 | |
| C. | NaCl溶液在电流的作用下电离成钠离子和氯离子 | |
| D. | 氯化钠晶体不导电是由于氯化钠晶体中不存在离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5mol | B. | 6.02×1023 | C. | 0.25mol | D. | 0.25g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青铜是我国使用最早的合金 | B. | 钢是用量最大、用途最广的合金 | ||
| C. | 合金的硬度一般高于各成分金属 | D. | 合金的熔点一般高于各成分金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 常温下有浓度为0.1mol/L,体积为VL的氨水,向其中逐滴加入一定浓度的盐酸,得到如图的滴定曲线,其中d点时两种溶液恰好完全反应.根据图象回答下列问题:
常温下有浓度为0.1mol/L,体积为VL的氨水,向其中逐滴加入一定浓度的盐酸,得到如图的滴定曲线,其中d点时两种溶液恰好完全反应.根据图象回答下列问题:| 离子浓度大小顺序 | 溶质化学式 | 溶液的pH |
| c (NH4+)>c (OH-)>c (CI-)>c (H+) | ① | >7 |
| ② | ③ | =7 |
| ④ | NH4Cl | ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,依图所示:
一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,依图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com