
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
| 盐酸液的体积(mL) | 30 | 30 | 30 | 30 |
| 样品(g) | 3.32 | 4.15 | 5.81 | 7.47 |
| 二氧化碳的体积(mL) | 672 | 840 | 896 | 672 |
分析 (1)由图表可知,二氧化碳的最大体积是896mL,即0.04mol,此时根据碳元素守恒,碳酸钠的质量是4.24g,当m(样品)≤4.24g时,样品质量与CO2体积成正比;
(2)3.32g样品中,n(NaHCO3)=2n(CO2)=2×$\frac{0.112L}{22.4L/mol}$=0.01mol,
n(H2O)=$\frac{0.45g-0.005mol×18g/mol}{18g/mol}$=0.02mol.
由碳元素守恒得:
n(Na2CO3)=$\frac{0.672L}{22.4L/mol}$-0.01mol=0.02mol,
结合物质的量比确定化学式;
(3)结合IV数据计算n(HCl),结合c=$\frac{n}{V}$计算;
(4)当生成二氧化碳的体积是0时,碳元素全部转化为碳酸氢钠,此时质量是3.36g,当4.24g≤m(样品)≤3.36g时,30mL盐酸全部参加反应.其中m(样品)=2.24g时,样品中Na2CO3、NaHCO3都恰好生成CO2;m(样品)=3.36g时,样品中Na2CO3恰好生成NaHCO3.
解答 解:(1)二氧化碳的最大体积是896mL,即0.04mol,根据碳元素守恒,此时只有碳酸钠,其质量是4.24g,m(样品)≤4.24g时,样品质量与CO2体积成正比.
设2.49g样品反应生成CO2的体积为V,
则$\frac{2.49}{V}$=$\frac{3.32g}{672mL}$,解得V=504mL,
故答案为:504;
(2)3.32g样品中,n(NaHCO3)=2n(CO2)=2×$\frac{0.112L}{22.4L/mol}$=0.01mol,
n(H2O)=$\frac{0.45g-0.005mol×18g/mol}{18g/mol}$=0.02mol.
由碳元素守恒得:
n(Na2CO3)=$\frac{0.672L}{22.4L/mol}$-0.01mol=0.02mol,
则n(Na2CO3):n(NaHCO3):n(H2O)=0.02mol:0.01mol:0.02mol=2:1:2.
故该天然碱的组成为:2Na2CO3?NaHCO3?2H2O,
答:该天然碱的组成为:2Na2CO3?NaHCO3?2H2O;
(3)根据表中的数据知道,30mL HCl(aq)中所含HCl物质的量=$\frac{7.47g}{332g/mol}$×2+$\frac{672}{22400}$mol=0.075mol,所以盐酸浓度c(HCl)=$\frac{0.075mol}{0.03L}$=2.5mol/L,
故答案为:2.5;
(4)和30mLHCl(aq)完全反应的样品的质量:$\frac{0.075mol}{5}$×332g/mol=4.98g,样品中Na2CO3和盐酸反应完全生成NaHCO3时(没有CO2放出时),样品质量:$\frac{0.075mol}{2}$×332g/mol=12.45g,
当0<W<4.98时,V(CO2)=202.4W(mL),当4.98≤W≤12.45时,V(CO2)=1680-134.9W(mL),当W≥12.45,时,V(CO2)=0,
答:上述实验中CO2(标准状况)体积V(mL)与样品质量W(g)之间的关系式为:0<W<4.98时,V(CO2)=202.4W(mL),当4.98≤W≤12.45时,V(CO2)=1680-134.9W(mL),当W≥12.45,时,V(CO2)=0.
点评 本题考查测定物质含量的计算,为高频考点,把握物质的性质、发生的反应及物质的量关系为解答的关键,侧重分析与计算能力的考查,注意表格数据的分析与应用,题目难度较大.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:填空题
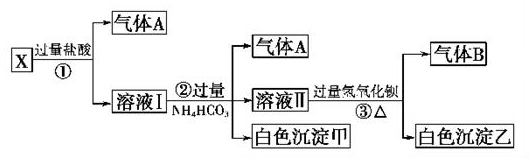
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
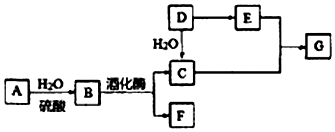
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
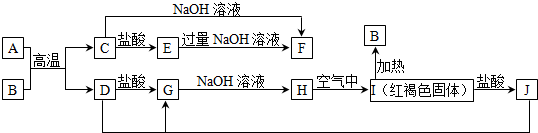
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
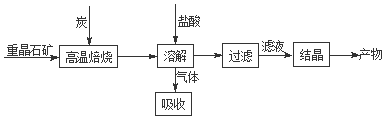
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15NA | B. | 0.6NA | C. | 1.2NA | D. | 2.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
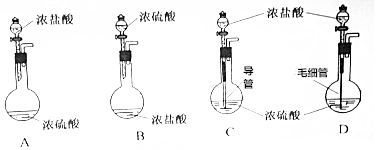
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
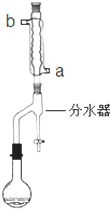 在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.实验步骤如下:
在苹果、香蕉等水果的果香中存在着乙酸正丁酯.某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯.实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
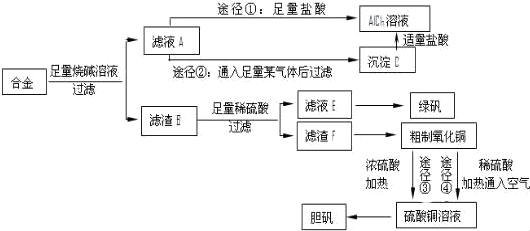
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com