
【题目】CO是生产羰基化学品的基本原料,对于以水煤气为原料提取CO的工艺,如果氢气未能充分利用,则提高了CO生产成本,所以在煤化工中常需研究不同温度下的平衡常数、投料比及热值问题.反应CO(g)+H2O(g)H2(g)+CO2(g)的平衡常数随温度的变化如表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | a |
(1)上述反应的逆反应是 ______ (填“放热”或“吸热”)反应.
(2)已知在一定温度下:C(s)+CO2(g)2CO(g)K
C(s)+H2O(g)H2(g)+CO(g)K1
CO(g)+H2O(g)H2(g)+CO2(g)K2
则K、K1、K2、之间的关系是 ______ .
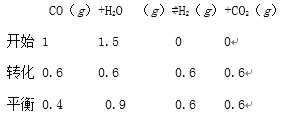
(3)800℃时,在2L的恒容密闭容器中,充入2.0molCO(g)和3.0molH2O(g),保持温度不变进行反应:CO(g)+H2O(g)H2(g)+CO2(g),4min时反应达到平衡,测得CO的转化率为60%.
①0~4min内,CO2的平均反应速率为 ______ molL-1min-1,800℃时a= ______ .
②800℃时四个不同容器中发生上述反应,测得各物质的浓度(molL-1)如表,其中达到平衡状态的是 ______ (填字母).
A | B | C | D | |
c(CO2) | 3 | 1 | 0.8 | 1 |
c(H2) | 2 | 1 | 0.8 | 1 |
c(CO) | 1 | 2 | 3 | 0.5 |
c(H2O) | 2 | 2 | 3 | 2 |
【答案】 吸热 K=![]() 0.15 1 D
0.15 1 D
【解析】试题分析:(1)根据表格数据,升高温度K减小,平衡逆向移动,正反应放热;(2)根据平衡常数表达式判断K、K1、K2、之间的关系;(3)根据“三段式”计算
①0~4min内,CO2的平均反应速率为,800℃时平衡常数.
②根据Q、K的关系判断是否达到平衡状态。
解析:升高温度K减小,平衡逆向移动,正反应放热,所以逆反应吸热;
(2)根据平衡常数表达式K=![]() 、K1=
、K1=![]() 、K2=
、K2=![]() ;所以K=
;所以K=![]() ;
;
(3) 
①0~4min内,CO2的平均反应速率为![]() 0.15 molL-1min-1;800℃时a=
0.15 molL-1min-1;800℃时a=![]() =
=![]() 1;
1;
②A、B、C、D的Q值分别为A、![]() ;B、
;B、![]() ;C、
;C、![]() ;D、
;D、![]() ,只有D中Q=K,故D达到平衡状态。
,只有D中Q=K,故D达到平衡状态。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】人造卫星常用的一种高能电池——银锌蓄电池,它在放电时的电极反应为:Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-,据此判断氧化银是
A. 负极,被氧化B. 正极,被还原
C. 负极,被还原D. 正极,被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属钨的晶胞结构模型图。实验测得金属钨的密度为19.3g.cm-3,钨的相对原子质量为183.9.假定金属钨为等径的刚性球。(必须列式计算)

(1)每个晶体分摊到的钨原子个数;
(2)计算晶胞的边长a和钨的原子半径r;
(3)计算金属钨晶胞的空间利用率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 碱性:LiOH>NaOH>KOH>RbOH
B. 金属性:Rb>K>Na>Li
C. 铷比钾活泼,铷能从氯化钾溶液中置换出钾
D. 铷不易与水反应放出氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知无水AlCl3遇潮湿空气即产生大量白雾,实验室可用如图所示装置制备AlCl3.

(1)装置A中发生反应的化学方程式为________________________________________.
(2)装置B盛放的试剂是______,其作用是_______________________________;装置C盛放的试剂是______,其作用是____________________________________.
(3)装置G的作用是________________,G中发生反应的化学方程式是_______.
(4)F中盛放的试剂是______,其作用是___________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是目前人类使用量最大的金属,它能形成多种化合物。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集的气体体积均小于2.24 L(标准状况),最主要的原因是_____________________;所得溶液在长时间放置过程中会慢慢出现浅黄色,试用离子方程式解释这一变化的原因:___________。
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox和用于除去废气的转化关系为ZnFe2O4![]() ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为________。请写出 ZnFe2Ox与NO2反应的化学方程式:_________________________(x用前一问求出的具体值)。
ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为________。请写出 ZnFe2Ox与NO2反应的化学方程式:_________________________(x用前一问求出的具体值)。
(3)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,该反应还生成一种可燃性气体,则反应的化学方程式为___________________________。
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开)工作原理为FePO4+Li![]() LiFePO4。则放电时正极上的电极反应式为___________________________________。
LiFePO4。则放电时正极上的电极反应式为___________________________________。
(4)已知25 ℃时Ksp[Fe(OH3)]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入______ mL 2 mol·L-1的盐酸(忽略加入盐酸时溶液体积的变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. CO2、H2S、NH3都是非电解质
B. 酸性氧化物不一定都是非金属氧化物
C. 强酸、强碱、盐都是离子化合物
D. FeBr3、FeCl2、CuS都不能直接用化合反应制备
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如图所示。下列有关说法错误的是
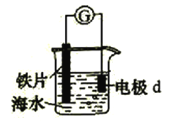
A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2+ 2H2O + 4e = 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H++ 2e = H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A. 28 g氮气含有的原子数为NA
B. 标准状况下,22.4 L 水中含有的水分子数为NA
C. 1 molOHˉ含有的电子数为10NA
D. 0.1 L 1 mol /L NaCl溶液中含有Na+个数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com