
根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
A.Cl2>I2>FeCl3>H2SO4 B.FeCl3>Cl2>I2>H2SO4
C.Cl2>FeCl3>H2SO4>I2 D.Cl2>FeCl3>I2>H2SO4
科目:高中化学 来源:2016-2017学年福建省高一上期中化学卷(解析版) 题型:选择题
将15%的NaOH溶液蒸发掉100g水后得到质量分数为30%体积为95mL的NaOH溶液,则此时溶液的物质的量浓度为( )
A.7.9mol/L B.6.25mol/L C.6.75 mol/L D.7 mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高二上学期期中化学试卷(解析版) 题型:填空题
运用元素周期律研究元素及其化合物的性质具有重要的意义.
I.部分短周期主族元素的最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的PH和原子序数的关系如图所示.
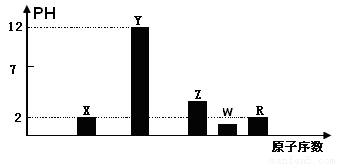
(1)元素R在周期表中的位置是
(2)元素Y和W形成的Y2W2型化合物中含有化学键的类型为
(3)请写出X的最高价氧化物对应的水化物与其气态氢化物的离子反应方程式
Ⅱ.短周期元素C、O、S能形成多种化合物,如CO2、CS2、COS等
(1)下列能说明碳、硫两种元素非金属性相对强弱的是 (填序号)
A.S与H2发生化合反应比C与H2化合更容易
B.酸性:H2SO3>H2CO3
C.稳定性:CH4<H2S
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害,其分子结构和CO2相似
①羰基硫(COS)的电子式为:
②羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下:
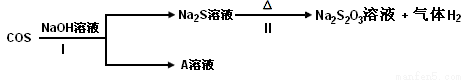
已知A是一种正盐,则反应I的化学反应方程式为
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高二上学期期中化学试卷(解析版) 题型:选择题
对于化学反应3W(g)+2X(g) 4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
A.V(W) = 3V(Z) B.2V(X) = 3V(Z) C.2V(X) = V(Y) D.3V(W) = 4V(Y)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省辽源市高一上学期期中化学卷(解析版) 题型:实验题
有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种.现进行如下实验:
①取少量固体粉末,加入盛有足量水的烧杯中,充分搅拌静置后,底部白色沉淀,上层为无色溶液;
②继续往烧杯中加入足量稀硝酸,白色沉淀完全消失;并有气泡产生;
③取少量②中溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
(1)根据以上实验现象可知,该白色固体中一定含有 ,(填化学式,下同)一定不含有 ,可能含有 ;
(2)上述实验②过程中所发生反应的离子方程式为: ;
(3)上述实验③过程中所发生反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省辽源市高一上学期期中化学卷(解析版) 题型:选择题
在酸性的无色透明溶液中能够大量共存的是
A.NH4+ 、Fe3+、SO42-、Cl- B.Mg2+、Ag+、CO32-、Cl-
C.K+、NH4+、SO42-、Cl- D.K+、Na+、NO3-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省辽源市高一上学期期中化学卷(解析版) 题型:选择题
下列反应能用H++OH-==H2O 表示的是
A.NaOH 溶液和CO2 的反应 B.Ba(OH)2 溶液和稀H2SO4 的反应
C.NaHSO4 溶液和KOH 反应 D.石灰乳和稀H2SO4 的反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省娄底市等五校高一上期中化学卷(解析版) 题型:选择题
分析离子反应xR2++yH++O2=mR3++nH2O,下列说法中正确的是( )
)
A.n=2,H2O是氧化产物
B.x=y=m=4
C.该反应中R2+得到电子,被氧化为R3+
D.任何氧化还原反应中氧化剂失电子总数都等于还原剂得电子总数
查看答案和解析>>
科目:高中化学 来源:2016-2017学年海南省高二上期中文化学卷(解析版) 题型:填空题
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明。请根据此表,结合初中化学和生物学科的知识,回答下列问题。
配料表 | 精制海盐、碘酸钾 |
含碘量 | 20~40mg/kg |
卫生许可证号 | ××卫碘字(1999)第001号 |
分装日期 | 见封底 |
储藏方法 | 密封、避光、防潮 |
食用方法 | 烹调时,待食品熟后加入碘盐 |
(1)要在食盐中加碘,是因为碘是人体内合成________激素的主要原料,缺碘会引起疾病。
(2)食盐中加碘,这碘指的是__________(填元素、原子或单质)
(3)碘酸钾的化学式为KIO3,其中碘元素的化合价为__________。
(4)根据碘盐的食用方法可推测碘元素的化学性质,碘酸钾在受热时容易___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com