
| A. | 简单离子半径:乙>丙>丁 | |
| B. | 最高价氧化物对应的水化物的碱性:乙>丙 | |
| C. | 简单气态氢化物稳定性:丁>甲 | |
| D. | 甲和丁组成的化合物在熔融状态下可以导电 |
分析 短周期元素甲、乙、丙、丁的原子序数依次增大,甲的L层电子数是K层的3倍,则L呈含有6个电子,甲为O元素;丁所在族序数是周期数的2倍,由于原子序数丁最大,则丁只能位于第三周期,丁的族序数为3×2=6,则丁为S元素;乙、丙、丁的最外层电子数之和为10,则乙、丙的最外层电子数之和=10-6=4,乙、丙的原子序数大于O元素,则乙的最外层电子数只能为1、丙的最外层电子数为3,则乙为Na元素,丙为Al元素,据此进行解答.
解答 解:短周期元素甲、乙、丙、丁的原子序数依次增大,甲的L层电子数是K层的3倍,则L呈含有6个电子,甲为O元素;丁所在族序数是周期数的2倍,由于原子序数丁最大,则丁只能位于第三周期,丁的族序数为3×2=6,则丁为S元素;乙、丙、丁的最外层电子数之和为10,则乙、丙的最外层电子数之和=10-6=4,乙、丙的原子序数大于O元素,则乙的最外层电子数只能为1、丙的最外层电子数为3,则乙为Na元素,丙为Al元素,
A.离子的电子层越多,离子半径越大,电子层相同时,核电荷数越大,离子半径越小,则离子半径大小为:丁>乙>丙>,故A错误;
B.金属性乙大于丙,则最高价氧化物对应的水化物的碱性:乙>丙,故B正确;
C.非金属性甲大于丁,简单气态氢化物稳定性:丁<甲,故C错误;
D.甲和丁组成的化合物二氧化硫或三氧化硫,二者都是共价化合物,在熔融状态下不会导电,故D错误;
故选B.
点评 本题考查了原子结构与元素周期律的应用,题目难度中等,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol/L的NaHCO3溶液中HCO3-和CO3 2-离子数之和为0.1NA | |
| B. | 标准状况下,22.4LC2H4与C3H6混合气体所含有分子数为NA | |
| C. | 1molNa2O2与足量的CO2反应转移的电子数为2NA | |
| D. | 18gNH4+所含的电子数11NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 这类电池的正极反应与金属的吸氧腐蚀正极反应相似 | |
| B. | 每转移1mol电子则这种电池产生电能为0.5度电 | |
| C. | 电池的负极反应为:CH4+10OH-═CO32-+7H2O+8e- | |
| D. | 当消耗0.4mol燃料时,电池中的各种离子的浓度关系为:C(K+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.4g乙烯与丙烯的混合气体含有NA个碳原子 | |
| B. | 精炼铜,若阳极失去2NA个电子,则阴极增重64g | |
| C. | 在1L 0.1mol/L的Na2CO3溶液中,阴离子总数小于0.1NA | |
| D. | 将1L 2mol/L的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 15ml 0.1mol/L KOH溶液中滴入0.2mol/L(一元弱酸HA),溶液pH和加入弱酸HA体积的关系曲线如图所示,有关离子浓度的大小关系正确的是( )
15ml 0.1mol/L KOH溶液中滴入0.2mol/L(一元弱酸HA),溶液pH和加入弱酸HA体积的关系曲线如图所示,有关离子浓度的大小关系正确的是( )| A. | 在A、B间任意一点(不包括A、B两点):c(K+)>c(A-)>c(OH-)>c(H+) | |
| B. | 在B点:c(A-)=c(K+)>c(OH-)=c(H+),且a=7.5 | |
| C. | 在C点:c(A-)>c(K+)>c(OH-)>c(H+) | |
| D. | 在D点:c(A -)+c(HA)>2 c(K+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.35kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
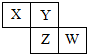
| A. | W的原子序数不可能是X的原子序数的3倍 | |
| B. | Z元素可能是金属元素 | |
| C. | W的气态氢化物的稳定性一定比Y的强 | |
| D. | 四种元素的原子有可能均能与氢原子形成18电子分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Y>Z>X | |
| B. | 标准状况下的2.24 LM溶于水,所得溶液pH=13 | |
| C. | YZ2能使湿润的淀粉KI试纸变蓝 | |
| D. | 一定条件下,Cu可与W的最高价氧化物对应水化物发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com