
【题目】KClO3 和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯(ClO2)气体,该反 应的化学方程式为 2 KClO3 + 4HCl(浓) = 2 KCl + 2ClO2↑ + Cl2↑ + 2H2O。
(1)该反应的氧化产物是_____(填化学式)。
(2)在反应中浓盐酸表现出来的性质是_____(填字母)。
A.只有还原性 B.只有氧化性 C.还原性和酸性 D.氧化性和酸性
(3)若该反应产生 2.24 L(标准状况)ClO2,则转移电子的物质的量为_____。
(4)Cl2、H2O2、ClO2(还原产物为 Cl-)、O3(1 mol O3 转化为 1 mol O2 和 1 mol H2O)等物质常 被用作消毒剂。等物质的量的上述物质消毒效率最高的是_____(填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
【答案】Cl2 C 0.lmol C
【解析】
对于反应2KClO3 + 4HCl(浓) = 2 KCl + 2ClO2↑ + Cl2↑ + 2H2O,
(1) KClO3为氧化剂,HCl为还原剂,该反应的氧化产物是含有化合价升高元素的生成物。
(2)在反应中,浓盐酸生成KCl 和 Cl2,其中生成KCl的盐酸没有发生价态变化,生成Cl2的盐酸价态升高。
(3)该反应中,KClO3 得电子生成ClO2,由产生 2.24 L(标准状况)ClO2,可计算出转移电子的物质的量。
(4)分析Cl2、H2O2、ClO2(还原产物为 Cl-)、O3(1 mol O3 转化为 1 mol O2 和 1 mol H2O)等物质作消毒剂后,所得产物中变价元素的价态,得出1mol物质得电子的物质的量,得电子数目最多的物质,消毒效率最高。
(1) KClO3为氧化剂,HCl为还原剂,该反应的氧化产物为Cl2;答案为:Cl2;
(2)在反应中,浓盐酸生成KCl 和 Cl2,其中生成KCl的盐酸没有发生价态变化,表现出酸性,生成Cl2的盐酸价态升高,表现出还原性;答案为:C;
(3)KClO3+e-→ClO2,n(ClO2)=![]() =0.1mol,则转移电子的物质的量为0.1mol;答案为:0.1mol;
=0.1mol,则转移电子的物质的量为0.1mol;答案为:0.1mol;
(4) Cl2+2e-→2Cl-,H2O2+2e-→2H2O,ClO2+5e-→Cl-、O3+2e-→O2+H2O,从关系式可以看出,1mol物质中,获得电子数目最多的物质为ClO2,则消毒效率最高的物质是ClO2;答案为:C。


科目:高中化学 来源: 题型:
【题目】已知: +4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O。可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点为9.79℃、131.4℃,不溶于水);试管d中装有适量液溴(表面覆盖少量水)。
+4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O。可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点为9.79℃、131.4℃,不溶于水);试管d中装有适量液溴(表面覆盖少量水)。
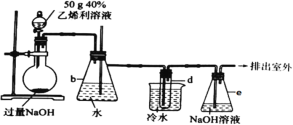
(1)e装置的作用是_______________;当观察到______________________________现象时,试管d中反应基本结束。
(2)若用冰水代替烧杯中的冷水,可能引起的不安全后果是_________________________。
(3)实验结束后精制试管d中粗产品,操作先后顺序是___________________。
A.蒸馏 B.水洗 C.用干燥剂干燥 D.10%NaOH溶液洗
(4)实验消耗40%乙烯利溶液50g,制得产品mg,则乙烯利合成1,2-二溴乙烷的产率为________________(列出含m的计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把7.5 g镁铝合金的粉末放入200ml 4mol/L的盐酸中,往充分反应后的混合溶液中逐渐滴入一定物质的量浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如图所示。

(1)合金中镁的物质的量为_______。
(2)氢氧化钠的物质的量浓度为_______mol/L。
(3)V1=_______mL。
(4)写出该合金溶于足量NaOH溶液的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2的一些性质或用途如图,下列说法正确的是( )
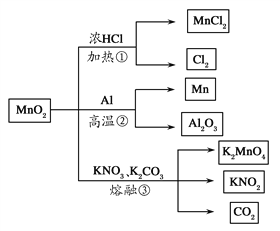
A. ①、②、③三个反应中MnO2均作氧化剂
B. 足量MnO2与2 L 10 mol/L HCl共热,可生成5 mol Cl2
C. 反应②若生成1 mol Al2O3,则反应过程中转移12 mol电子
D. 反应③中K2CO3和KNO3的化学计量数均为1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向四只盛有不同溶液的烧杯中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图(忽略CO2的溶解和HCl的挥发):
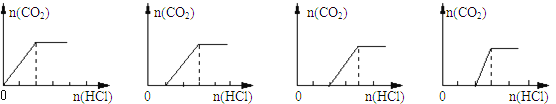
则下列分析都正确的组合是( )
①I图对应溶液中的溶质为NaHCO3
②II图对应溶液中的溶质为Na2CO3和NaHCO3,且二者的物质的量之比为1:1
③III图对应溶液中的溶质为NaOH和Na2CO3,且二者的物质的量之比为1:1
④IV图对应溶液中的溶质为Na2CO3
A.①② B.①③ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验仪器,用图中的实验装置进行实验,证明过氧化钠可作供氧剂。
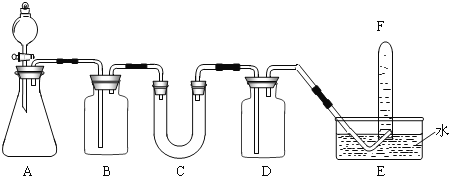
(1)A 是制取 CO2 的装置,可选用的试剂_____(填序号)
①碳酸钙固体与稀硫酸 ②碳酸钠固体与稀盐酸 ③碳酸氢钠固体与氢氧化钠溶液
写出对应的离子方程式_________________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和 NaHCO3 溶液 | ____________ |
C | ____________ | 与 CO2 和水反应产生 O2 |
D | NaOH 溶液 | ____________ |
(3)写出过氧化钠与二氧化碳反应的化学方程式_____。
(4)用_____检验 F 中收集到的气体,现象是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)原子序数大于4的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,据此推断:
①A和B所属周期数之差为___________
②A和B的核电荷数之差为____________(用含m、n的代数式表示)
③B和A的族序数之差为______________(用含m、n的代数式表示)
(2)A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。回答下列问题:
①如果A和B同在ⅠA族,当B在A的上一周期时,B的原子序数为_____________;当B在A的下一周期时,B的原子序数为______________;
②如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________当B在A的下一周期时,B的原子序数为______________。
(3)某粒子的结构示意图为: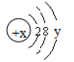 试回答:
试回答:
①当x-y=10时,该粒子为________(填“原子”或“阳离子”“阴离子”)
②当y=8时,该粒子可能是(写名称):_______、________、_______、_______、_______。
③写出y=3与y=7的元素最高价氧化物对应水化物发生反应的离子方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是25℃时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | 1.8×10-10 | 2.0×10-12 | 1.8×10-5 | 3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.碳酸钠溶液中滴加少量氯水的离子方程式H2O+CO32-+Cl2=HCO3-+Cl-+HClO
C.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COO-):c(CH3COOH)=9:5,此时溶液pH=5
D.向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol·L-1的AgNO3,CrO42-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体铝钠合金(钠和铝熔合而成)可用于核反应堆的载热介质。下列有关说法不正确的是( )
A.自然界中没有游离的钠和铝
B.若铝钠合金投入水中无固体剩余,则n(Al)≤n(Na)
C.铝钠合金投入到氯化铜溶液中,一定有氢氧化铜沉淀,也可能有铜析出
D.相同质量不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com