
����Ŀ����Ҫ�����
I��NaNO2 ����ۺ�ʳ�����ƣ�������ζ������ʹ����ʳ�ж�����֪ NaNO2�ܷ�����Ӧ��2NaNO2��4HI=2NO����I2��2NaI��2H2O��
��1��������Ӧ���������� ________��
��2������������Ӧ������ NaNO2 �� NaCl����ѡ�õ������Т�ˮ���ڵ⻯��������ֽ�۵��ۡ��ܰơ���ʳ�ף�����Ϊ����ѡ�õ�������________(�����)��
��3������ƽ���»�ѧ����ʽ��____Al��____NaNO3��____ NaOH= ____NaAlO2��____ N2����___H2O��________________������Ӧ������ת�� 5 mol ���ӣ������ɱ�״���� N2 �����Ϊ_________L��
II����100mL1.5mol/L������������Һ�л���ͨ��һ������CO2����Ӧ����������Һ����λ����μ�һ��Ũ�ȵ����ᣬ���������������������������������������ܽ���ˮ����ϵ��ͼ��ʾ��
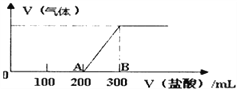
��:������������Һ��һ������CO2��ַ�Ӧ�����Һ������Ϊ____��д��ѧʽ����
�������Ũ��Ϊ_______��
��B��ʱ�������������ڱ�״���µ����Ϊ_______L��
���𰸡�NaNO2 �ڢ� 10 6 4 10 3 2 11.2 NaOH��Na2CO3 0.5mol/L 1.12
��������
���ݻ��ϼ۱仯�ж��������ͻ�ԭ�������ݵ�ʧ�����غ���ƽ������ԭ��Ӧ����ʽ������ͼ���е�����������Һ�����ʵ���ɣ��������ݷ���ʽ������ҺŨ�ȡ�
I����1���õ��ӵķ�Ӧ�������������õ��ӻ��ϼ۽��ͣ�����������Ӧ���������� NaNO2��
�ʴ�Ϊ��NaNO2��
��2�����������2NaNO2��4HI=2NO����I2��2NaI��2H2O��ʾ��������Һ��NaNO2�����������������ɵ��ʵ⣬���Լ���NaNO2 �� NaCl����ѡ�õ������Тڵ⻯��������ֽ�͢�ʳ�ף��ʴ�Ϊ���ڢݣ�
��3�����ݵ�ʧ�����غ���ƽ��ѧ����ʽΪ��10Al��6NaNO3��4NaOH=10NaAlO2��3N2����2H2O������ʽ�е�Ԫ�ػ��ϼ���+5����Ϊ0����������Ӧ������ת�� 5 mol ���ӣ�������0.5mol N2 �����״���µ��������Ϊ11.2L��
�ʴ�Ϊ��10,6,4,10,3,2��11.2��
II������ͼ��ʾ���ռ�������ʱ��δ���������ɣ�˵���������ƹ�����CO2��������NaOH��Ӧ������Na2CO3������δ��Ӧ��NaOH������Һ������ΪNaOH��Na2CO3��
�ʴ�Ϊ��NaOH��Na2CO3��
�ڼ�������200mLʱ��ʼ�������壬����������300mLʱ���ٲ������壬A��B�η���NaHCO3+HCl�TNaCl+H2O+CO2������O-A�����ĵ�����ΪA��B�Ķ�������Ӧ����ӦΪNaOH��Na2CO3�Ļ������߶��������ᷴӦ����Ӧ�����ӷ���ʽ�ֱ�Ϊ��OH-+H+�TH2O��CO32-+H+�THCO3-��B��ʱ��Һ�е����ʽ���NaCl������ԭ���غ�ã�c(HCl)0.3L=0.1L��1.5mol/L����c(HCl)=0.5mol/L��
�ʴ�Ϊ0.5 mol/L��
��AB������HClΪ0.1L��0.5mol/L=0.05mol����NaHCO3+HCl�TNaCl+H2O+CO2������֪���ɶ�����̼�����ʵ���Ϊ0.05mol�������0.1mol������̼�����Ϊ��22.4L/mol��0.05mol=1.12L��
�ʴ�Ϊ��1.12��


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ʵ�飬�䷽����ƺ�������
A | B | C | D |
����װ�������� | �ƹ������� | ��֤ŨH2SO4����ˮ�ԡ�ǿ������ | �Ƚ�NaHCO3��Na2CO3�ܽ�� |
|
|
|
|
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڹ���������˵������ȷ����(����)
A. �����������ᷴӦ�����ӷ���ʽ��SiO32����2H��=H2SiO3��
B. ��������Һ�׳ơ��ݻ��������Һ�Լ��ԣ��μӷ�̪�Ժ�ɫ
C. Na2CO3��SiO2 ![]() Na2SiO3��CO2����˵���������Ա�̼��ǿ
Na2SiO3��CO2����˵���������Ա�̼��ǿ
D. ˮ���������ڿ����б��ʣ���Ϊ������е�CO2������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ���������Ϊ��ѧ��ѧ�����Ĵ��������֮��������ͼ��ʾ�ķ�Ӧ��ϵ�����������鲻��������ת����ϵ����
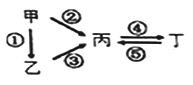
ѡ�� | �� | �� | �� | �� |
A | Fe | FeCl2 | FeCl3 | Fe(OH)3 |
B | Si | SiO2 | Na2SiO3 | Na2CO3 |
C | Na | Na2O | Na2O2 | NaOH |
D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I��������8���л��ﰴҪ������
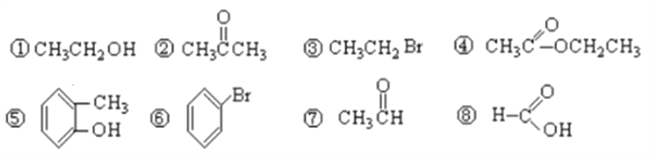
��1���������ŷ��࣬���������������___________������ţ������ڴ�����_________������ţ���
��2���������������ŵ�����_______________���������������Žṹ��ʽ_____________��
II�����и����е������л�������ǣ�A��ͬһ���� B��ͬϵ�� C��ͬ���칹�壬���ж�����֮��Ĺ�ϵ������ĸ�����գ���
��3��2-������Ͷ���_______________��
��4���������������_________________��
��5��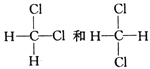 ______________��
______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ֿ���������A��B��C��D��E���������������������ӻ�����ͬ���ֱ�������������Al3����Fe3����Cu2����Ba2����K��������������NO![]() ��OH����Cl����CO
��OH����Cl����CO![]() ��Xn-(n=1��2)�е�һ�֡�
��Xn-(n=1��2)�е�һ�֡�
��1��ijͬѧͨ���ȽϷ�������Ϊ�������Ϳ��ж����б��е�����������_____��_____��
��2������C�к�������Xn-��Ϊ��ȷ��Xn-���ֽ�(1)�е��������ʼ�ΪA��B����C��A����Һ���ʱ������ɫ��������ó����е�������ϡHNO3�����������ܽ⣬ʣ���ɫ���壬��XΪ________(����ĸ)��
A��Br�� B��CH3COO�� C��SO![]() D��HCO
D��HCO![]()
��3����38.4 g CuͶ��װ������D��Һ���Թ��У�Cu���ܽ⣬�ٵμ�ϡH2SO4��Cu���ܽ⣬�ܿڸ����к���ɫ������֣�������Dһ���������������е�________(����Ӧ�����ӷ���)��д��Cu�ܽ�����ӷ���ʽ____________________________________________����Ҫ��Cu��ȫ�ܽ⣬���ټ���H2SO4�����ʵ�����_____________��
��4��E��Һ������ᷴӦʱ������ʹ���۱��������ʣ��÷�Ӧ�����ӷ���ʽΪ___________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. ̼��������ᷴӦ��CO32����2H+![]() CO2����H2O
CO2����H2O
B. ����Ͷ�뵽NaOH��Һ�У�2Al+2OH���T�T 2AlO2��+H2��
C. ��NaHCO3��Һ�м�������ij���ʯ��ˮ��2HCO3��+Ca2++2OH���TCaCO3��+2H2O+CO32��
D. ��������Һ�м�������������Һ��SO42��ǡ�ó�����Al3++2SO42��+2Ba2++4OH���T2BaSO4��+AlO2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£�ͬ����ļס��������������������17:14������������H2S���������岻������( )
A.N2B.HClC.C2H4D.CO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Fe3O4��һ�ָ��ӵĻ�����仯ѧʽ�ɸ�дΪFeO��Fe2O3������A�����ɵĺ�ɫ���ʣ�������ѧϰС����������ֲ�ͬ�IJ��룬������С��ͬѧ���е�ʵ�������̽�����������С���˼·����ʾ�����ؿհס�
�����룩���飺��ɫ������FeO
���飺��ɫ������Fe3O4
���飺_____________��
��ʵ��̽����
(1)������Ϊһ�ּ��Եķ��������жϼ��������ȡA�����ɵĺ�ɫ�����������ձ�����ϡ����ʹ����ȫ�ܽ⣬�ټ�______��Һ�Լ���Fe3�����۲쵽��Һ������_________�����жϡ�
(2)������Ϊ��ͨ�������ⶨ��ȷ��A�����ɵĺ�ɫ���ʵ���ɣ�����֤���������ȷ��ȡA�����ɵĺ�ɫ����2.32g�ܽ�������ϡ�������������ˮ��������ˮ��Ӧ�����ӷ���ʽΪ��_____________���ټ�������NaOH��Һ����ϴ�Ӻ�����ճ��������Ƶù�������Ϊ________�������ж�����ͬѧ������ȷ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com