
| A.从海带中提取碘单质的过程涉及氧化还原反应 |
| B.往淡水中加入NaCl等配成的人造海水,可用于海产品的长途运输 |
| C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的 |
| D.海洋经济专属区的资源开发可获得Fe、Co、K、Au、Mg、B等金属 |
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 344 mL | B.672 mL | C.大于1 344 mL | D.小于672 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制钛:用金属钠置换出氯化钛(TiCl4)溶液中的钛 |
| B.炼铁:用焦炭和空气反应产生的一氧化碳在高温下还原铁矿石中的铁 |
| C.制钠:用海水作原料制得精盐,再电解纯净氯化钠溶液得到金属钠 |
| D.炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸遇明火爆炸 |
| B.浓硫酸遇水发热爆炸 |
| C.铁与水(常温下)反应产生的氧化物爆炸 |
| D.稀释后的硫酸与铁反应产生的氢气在空气中遇明火而爆炸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

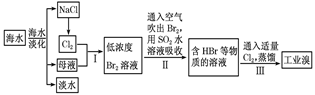
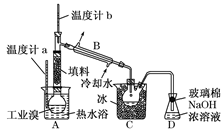
| A.制取NaHCO3的反应是利用其溶解度小于NaCl |
| B.用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C.在第③、④、⑤步骤中,溴元素均被氧化 |
| D.工业上通过电解饱和MgCl2溶液制取金属镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com