
| A. | 不能用手直接接触药品 | B. | 可用酒精灯对烧杯直接加热 | ||
| C. | 用鼻孔凑到容器口去闻气体的气味 | D. | 尝一下实验室里酒精的味道 |
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
CsICl2是一种碱金属的化合物,这类物质在化学反应中既可表现氧化性又可表现还原性,有关该物质的说法正确的是
A.Cs显+3价,I、Cl均显-1价
B.在CsICl2溶液中通入SO2气体,有硫酸生成
C.Cs显+1价,Cl显+1价,I显-3价
D.在CsICl2溶液中通入Cl2,有单质碘生成
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;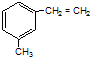 的名称为间甲基苯乙烯(3-甲基苯乙烯).
的名称为间甲基苯乙烯(3-甲基苯乙烯).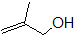 的分子式为:C4H8O.
的分子式为:C4H8O.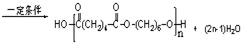 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 氢化物的沸点R>X | |
| B. | 原子半径:W>R>X | |
| C. | 气态氢化物的稳定性:X>Y | |
| D. | X、Z形成的化合物中可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积/mL | 20.05 | 20.00 | 18.80 | 19.95 |
| 醋酸浓度(mol•L-1 ) | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1 mol•L-1的NaOH溶液中氧原子个数为0.1NA | |
| B. | 常温常压下,15g甲基(-CH3)所含的中子数为9NA | |
| C. | 0.1 mol钠与足量O2充分反应时,转移的电子数为0.1NA | |
| D. | 0.2 mol SO2与0.1mol O2充分反应,产物的分子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com