
【题目】将足量CO2气体通入水玻璃中,然后加热蒸干,再在高温下充分灼烧,最后所得的固体物质是
A. 硅酸钠
B. 碳酸钠,硅酸钠
C. 碳酸钠,二氧化硅
D. 二氧化硅
科目:高中化学 来源: 题型:
【题目】现有反应m A(g)+n B(g) ![]() p C(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
p C(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
(1)该反应的逆反应是________热反应,且m+n______(填“>”“<”或“=”)p。
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则A的转化率________,B的转化率________。
(4)若升高温度,则化学平衡常数将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量________。
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色________,而维持容器内气体的压强不变,充入氖气时,混合物的颜色________(填“变浅”“变深”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O,Mr=990)简称三盐,白色或微黄色粉末,稍带甜味、有毒。200℃以上开始失去结晶水,不溶于水及有机溶剂。可用作聚氯乙烯的热稳定剂。以100.0吨铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。

已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13。
请回答下列问题:
(1)步骤①转化的目的是________。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是________(任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为________。
(3)滤液2中可循环利用的溶质为________(填化学式)。若步骤④沉铅后的滤液中c(Pb2+)=1.82×l0-5 mol·L-1,则此时 c(SO42-)=________mol·L-1。
(4)步骤⑥合成三盐的化学方程式为________。若得到纯净干燥的三盐49.5 t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下都是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态。下列说法正确的是
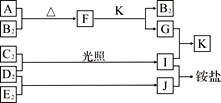
A. B氢化物的沸点高于其同主族其它元素氢化物的沸点
B. 原子半径大小:A>C>B>E>D
C. F中既含有离子键又含有极性共价键
D. G中的阴离子能抑制水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z组成的化合物Y2X和ZX2 , Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3 . 已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子的最外层电子数是次外层电子数的2倍.试回答:
(1)X,Y,Z元素的名称及符号.X:Y:Z:
(2)写出ZX2的化学式:
(3)写出Y2X对应水化物的电子式 , 并指出其中存在的化学键.
(4)写出Y2X溶于水的溶液与ZX2反应的化学方程式. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中能大量共存的离子组是
A. Al3+ H+ HCO3- Cl- B. Na+ AlO2- OH- SO42-
C. Ca2+ K+ NO3- CO32- D. H+ Fe2+ MnO4- NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)在反应A(g)+3B(g)═2C(g)中,若以物质A表示的该反应的化学反应速率为0.2molL﹣1min﹣1 , 则以物质B表示此反应的化学反应速率为molL﹣1min﹣1 .
(2)在2L的密闭容器中,充入2mol N2和3mol H2 , 在一定条件下发生反应,3s后测得N2为1.9mol,则以H2的浓度变化表示的反应速率为 .
(3)将10mol A和5mol B放入容积为10L的密闭容器中,某温度下发生反应:3A(g)+B(g)═2C(g),在最初2s内,消耗A的平均速率为0.06molL﹣1s﹣1 , 则在2s时,容器中此时C的物质的量浓度为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com