
£Ø14·Ö£©ŅŃÖŖ£ŗAĪŖŗ¬½šŹōĄė×ӵĵ»ĘÉ«¹ĢĢå»ÆĢØĪļ£¬E”¢XĪŖæÕĘųÖŠ³£¼ūĘųĢ壬A”¢B”¢C”¢Dŗ¬ÓŠĻąĶ¬µÄ½šŹōĄė×Ó£¬Ęä×Ŗ»Æ¹ŲĻµČēĻĀĶ¼£Ø²æ·Ö²śĪļŅŃĀŌČ„£©”£
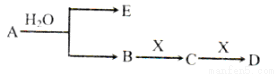
Ēė»Ų“šĻĀĮŠĪŹĢā
£Ø1£©ÕāÖÖ½šŹōĄė×ӵĥė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ_____________;
£Ø2£©XµÄµē×ÓŹ½_______________;
£Ø3£©BÖŠĖłŗ¬»Æѧ¼üµÄĄąŠĶŹĒ_____________;
³£ĪĀ³£Ń¹ĻĀ£¬7.8gAÓė×ćĮæµÄĖ®³ä·Ö·“Ó¦·Å³öČČĮæa kJ£¬Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½
_________________________________________________________________.
£Ø4£©¢ŁCŅ²æÉ×Ŗ»ÆĪŖB£¬Š“³öøĆ×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½_______________________________;
¢ŚBÓėD·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_______________________________________.
£Ø5£©½«Ņ»¶ØĮæµÄĘųĢåXĶØČė2LBµÄČÜŅŗÖŠ£¬ĻņĖłµĆČÜŅŗÖŠ±ßÖšµĪ¼ÓČėĻ”ŃĪĖį±ßÕńµ“ÖĮ¹żĮ棬²śÉśµÄĘųĢåÓėŃĪĖįĪļÖŹµÄĮæµÄ¹ŲĻµČēĶ¼£ØŗöĀŌĘųĢåµÄČܽāŗĶHClµÄ»Ó·¢£©”£
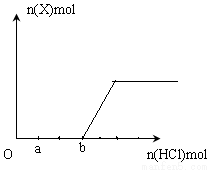
Ēė»Ų“š£ŗaµćČÜŅŗÖŠĖłŗ¬ČÜÖŹµÄ»ÆѧŹ½ĪŖ__________ £¬a£bÖ®¼äµÄ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ_________________________”£
£Ø14·Ö£©
£Ø1£©Na+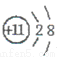 (1·Ö)
(1·Ö)
£Ø2£©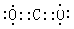 (1·Ö)
(1·Ö)
£Ø3£©£Ø¼«ŠŌ£©¹²¼Ū¼ü”¢Ąė×Ó¼ü£Ø2·Ö£©2Na2O2(s)+2H2O(l)=4NaOH(aq)+ O2(g)”ü”÷H=-20akJ/mol(2·Ö)
£Ø4£©¢ŁCa(OH)2+Na2CO3=CaCO3”ż+2NaOH»ņ Ba(OH)2+Na2CO3=BaCO3”ż+2NaOH
(2·Ö)
¢ŚOH-+HCO3-=CO32-+ H2O(2·Ö)
£Ø5£©Na2CO3”¢NaCl (2·Ö) CO32- + H+ = HCO3-(2·Ö)
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©µ»ĘÉ«¹ĢĢå»ÆŗĻĪļŹĒ¹żŃõ»ÆÄĘ¹ĢĢ壬ĖłŅŌAŹĒ¹żŃõ»ÆÄĘ£¬ÓėĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘÓėŃõĘų£¬ŌņEŹĒŃõĘų£¬BŹĒĒāŃõ»ÆÄĘ£¬ĒāŃõ»ÆÄĘÓėæÕĘųÖŠµÄ¶žŃõ»ÆĢ¼·“Ó¦£¬ĖłŅŌXŹĒ¶žŃõ»ÆĢ¼£¬CŹĒĢ¼ĖįÄĘ£¬DŹĒĢ¼ĖįĒāÄĘ”£ŌņA ÖŠµÄ½šŹōŃōĄė×ÓŹĒÄĘĄė×Ó£¬Ąė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖNa+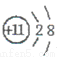 £»
£»
£Ø2£©XŹĒ¶žŃõ»ÆĢ¼ŹōÓŚ¹²¼Ū»ÆŗĻĪļ£¬µē×ÓŹ½ĪŖ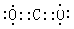
£Ø3£©BŹĒNaOH£¬¼ČÓŠĄė×Ó¼üÓÖÓŠ¹²¼Ū¼ü£»7.8gµÄ¹żŃõ»ÆÄʵÄĪļÖŹµÄĮæŹĒ0.1mol£¬ĖłŅŌ1mol¹żŃõ»ÆÄĘÓė×ćĮæĖ®·“Ó¦·Å³ö10akJµÄČČĮ棬Ōņ¹żŃõ»ÆÄĘÓėĖ®·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ2Na2O2(s)+2H2O(l)=4NaOH(aq)+ O2(g)”ü”÷H=-20akJ/mol£»
£Ø4£©¢ŁĢ¼ĖįÄĘ×Ŗ»ÆĪŖĒāŃõ»ÆÄĘ£¬·¢Éśø“·Ö½ā·“Ó¦£¬Ģ¼ĖįÄĘÓėĒāŃõ»ÆøĘ£Ø»ņĒāŃõ»Æ±µ£©ČÜŅŗ·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĒāŃõ»ÆÄĘ£¬Ąė×Ó·½³ĢŹ½ĪŖCa(OH)2+Na2CO3=CaCO3”ż+2NaOH£»
¢ŚĒāŃõ»ÆÄĘÓėĢ¼ĖįĒāÄĘ·“Ӧɜ³ÉĢ¼ĖįÄĘŗĶĖ®£¬Ąė×Ó·½³ĢŹ½ĪŖOH-+HCO3-=CO32-+ H2O£»
£Ø5£©ÓÉĶ¼æÉÖŖ£¬HClÓėĢ¼ĖįÄĘ·“Ó¦ĻČÉś³ÉĢ¼ĖįĒāÄĘ£¬ŌŁÉś³É¶žŃõ»ÆĢ¼£¬Éś³ÉĢ¼ĖįĒāÄĘŗĶÉś³É¶žŃõ»ÆĢ¼ĻūŗĵÄHClµÄĪļÖŹµÄĮæŹĒĻąĶ¬µÄ£¬¶ųĶ¼ÖŠÉś³É¶žŃõ»ÆĢ¼ĘųĢåĒ°ĻūŗĵÄHClÓėÉś³É¶žŃõ»ÆĢ¼ĻūŗĵÄHClµÄĪļÖŹµÄĮæÖ®±ČŹĒ3:2£¬ĖµĆ÷¶žŃõ»ÆĢ¼ÓėĒāŃõ»ÆÄĘ·“Ó¦ÖŠĒāŃõ»ÆÄĘ¹żĮ棬ĖłŅŌaµć“ś±ķHClÓėĒāŃõ»ÆÄĘ·“Ó¦£¬ČÜÖŹŹĒNa2CO3”¢NaCl£¬a£bÖ®¼äŹĒĢ¼ĖįÄĘÓėHCl·“Ӧɜ³ÉĢ¼ĖįĒāÄĘµÄ¹ż³Ģ£¬Ąė×Ó·½³ĢŹ½ĪŖCO32- + H+ = HCO3-”£
æ¼µć£ŗæ¼²éĪļÖŹĶʶĻ£¬¹żŃõ»ÆÄĘ”¢Ģ¼ĖįÄĘ”¢Ģ¼ĖįĒāÄĘ”¢¶žŃõ»ÆĢ¼µÄ»ÆѧŠŌÖŹ£¬Ąė×Ó·½³ĢŹ½µÄŹéŠ“£¬¶ŌĶ¼ĻńµÄ·ÖĪö


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ĖÄ“ØŹ”³É¶¼ŹŠĪ劣ø߶žĻĀѧʌʌ֊ĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆѧÓėÉś²ś”¢Éś»īĆÜĒŠĻą¹Ų£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø £©
A. Ź³Ę·±£ĻŹÄ¤°“²ÄÖŹ·ÖĪŖ¾ŪŅŅĻ©”¢¾ŪĀČŅŅĻ©£¬ĖüĆĒ¶¼ŹōÓŚĮ“דøß·Ö×Ó£¬ŹÜČČŅ×ČŪ»Æ
B. Ź³ÓĆÖ²ĪļÓĶµÄÖŲŅŖ³É·ÖŹĒøß¼¶²»±„ŗĶÖ¬·¾ĖįøŹÓĶõ„£¬ŹĒČĖĢåµÄÓŖŃųĪļÖŹ
C. ČĖŌģĻĖĪ¬”¢ŗĻ³ÉĻĖĪ¬ŗĶ¹āµ¼ĻĖĪ¬¶¼ŹĒÓŠ»śøß·Ö×Ó»ÆŗĻĪļ£¬·ūŗĻCn(H2O)mµÄ×é³É
D. æŲÖĘŗ¬Į×Ļ“µÓ¼ĮµÄŹ¹ÓĆ£¬ĪŖĮĖ·ĄÖ¹Ė®Ģåø»ÓŖŃų»Æ£¬±£»¤Ė®×ŹŌ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ĖÄ“ØŹ”ŅĖ²żŹŠ“ŗ¼¾ĘŚÖŠæ¼ŹŌø߶ž»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
LiFePO4µē³Ų¾ßÓŠĪČ¶ØŠŌøß”¢°²Č«”¢¶Ō»·¾³ÓŃŗƵČÓÅµć£¬æÉÓĆÓŚµē¶ÆĘū³µ”£µē³Ų·“Ó¦ĪŖ£ŗ
FePO4£«Li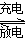 LiFePO4£¬µē³ŲµÄÕż¼«²ÄĮĻŹĒLiFePO4£¬øŗ¼«²ÄĮĻŹĒŹÆÄ«£¬ŗ¬Li£«µ¼µē¹ĢĢåĪŖµē½āÖŹ”£
LiFePO4£¬µē³ŲµÄÕż¼«²ÄĮĻŹĒLiFePO4£¬øŗ¼«²ÄĮĻŹĒŹÆÄ«£¬ŗ¬Li£«µ¼µē¹ĢĢåĪŖµē½āÖŹ”£
ĻĀĮŠÓŠ¹ŲLiFePO4µē³ŲĖµ·ØÕżČ·µÄŹĒ
A£®æɼÓČėĮņĖįŅŌĢįøßµē½āÖŹµÄµ¼µēŠŌ B£®·ÅµēŹ±Li£«Ļņøŗ¼«ŅʶÆ
C£®³äµē¹ż³ĢÖŠ£¬µē³ŲÕż¼«²ÄĮĻµÄÖŹĮæ¼õÉŁ D£®·ÅµēŹ±µē³ŲÕż¼«·“Ó¦ĪŖ£ŗLi-e£=== Li£«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ĖÄ“ØŹ”øßČż5ŌĀ³å“Ģ¾ķĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
£Ø13·Ö£©Įņ“śĮņĖįÄĘ£ØNa2S2O3£©Ė׳Ęŗ£²Ø£¬ĖüæÉæ“³ÉŹĒÓĆŅ»øöSŌ×ÓČ”“śĮĖNa2SO4ÖŠµÄŅ»øöOŌ×Ó¶ųŠĪ³ÉµÄ”£Ä³Š£»Æѧъ¾æŠŌѧĻ°Š”×éÓĆĄą±ČѧĻ°Ė¼Ļė£¬²¢ĶعżŹµŃéĢ½¾æNa2S2O3µÄ»ÆѧŠŌÖŹ”£
”¾Ģį³öĪŹĢā”æNa2S2O3ÓėNa2SO4½į¹¹ĻąĖĘ£¬»ÆѧŠŌÖŹŹĒ·ńŅ²ĻąĖĘÄŲ£æ
”¾ŹµŃéĢ½¾æ”æČ”ŹŹĮæNa2S2O3¾§Ģ壬ČÜÓŚĖ®ÖĘ³ÉNa2S2O3ČÜŅŗ£¬½ųŠŠČē±ķĖłŹ¾µÄĢ½¾æ£¬Ķź³É±ķÖŠÓŠ¹ŲÄŚČŻ”£
ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ĻÖĻó½āŹĶ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£© |
Ģ½¾æ¢ŁA. B.ĻņpH£½2µÄĮņĖįÖŠµĪ¼ÓNa2S2O3ČÜŅŗ | a.ČÜŅŗpH£½8 b. | i. ii. S2O32£+2H |
Ģ½¾æ¢ŚC.ĻņŠĀÖĘĀČĖ®£ØpH£¼2£©ÖŠµĪ¼ÓÉŁĮæNa2S2O3ČÜŅŗ | c.ĀČĖ®ŃÕÉ«±äĒ³ | iii. |
”¾ŹµŃé½įĀŪ”æĢ½¾æ¢Ł Ģ½¾æ¢Ś ”£
øł¾ŻĢ½¾æ¢ŁŗĶĢ½¾æ¢ŚµÄ½įĀŪ£¬Na2S2O3ŗĶNa2SO4»ÆѧŠŌÖŹ ”£
”¾ĪŹĢāĢÖĀŪ”æ
£Ø1£©¼×Ķ¬Ń§ĻņĢ½¾æ¢Ś·“Ó¦ŗóµÄČÜŅŗÖŠµĪ¼ÓAgNO3ČÜŅŗ£¬³öĻÖ°×É«³Įµķ£¬¾Ż“Ė¼×Ķ¬Ń§ČĻĪŖĀČĖ®æɽ«Na2S2O3Ńõ»Æ”£ÄćČĻĪŖ“Ė·½°øŹĒ·ńÕżČ·²¢ĖµĆ÷ĄķÓÉ£ŗ ”£
£Ø2£©ĒėÄćÖŲŠĀÉč¼ĘŅ»øöŹµŃé·½°ø£¬Ö¤Ć÷Na2S2O3Äܱ»ĀČĖ®Ńõ»Æ”£ÄćÉč¼ĘµÄ·½°øŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ĖÄ“ØŹ”øßČż5ŌĀ³å“Ģ¾ķĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·š¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®0.2mol/LNa2SČÜŅŗÖŠŗ¬ÓŠS2-ŹżÄæĪŖ0.2NA
B£®ŗ¬1molH2SO4µÄÅØĮņĖįŗĶ×ćĮæµÄĶĶźČ«·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ2NA
C£®Ä³ĆܱÕČŻĘ÷Ź¢ÓŠ0.1molN2£¬0.3molH2£¬ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.6NA
D£®³£ĪĀ³£Ń¹ĻĀ5.6gŅŅĻ©ŗĶ»·±ūĶéµÄ»ģŗĻĪļÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹżĪŖ0.4NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲČČ»Æѧ·½³ĢŹ½µÄ±ķŹ¾¼°Ėµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ŅŃÖŖC£ØŹÆÄ«£¬s£©= C£Ø½šøÕŹÆ£¬s£© ”÷H£¾0£¬Ōņ½šøÕŹÆ±ČŹÆÄ«ĪȶØ
B£®ŅŃÖŖI2£Øg£©£«H2£Øg£©=2HI£Øg£© ”÷H1£»I2£Øs£©£«H2£Øg£©=2HI£Øg£© ”÷H2£»
Ōņ”÷H1£¼”÷H2
C£®HClŗĶNaOH·“Ó¦µÄÖŠŗĶČČ”÷H=£57£®3kJ/mol£¬ŌņH2SO4ŗĶBa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø£57£®3£©kJ/mol
D£®ŅŃÖŖH2£Øg£©£«F2£Øg£©=2HF£Øg£© ”÷H=£270kJ/mol£¬Ōņ2L·ś»ÆĒāĘųĢå·Ö½ā³É1LĒāĘųŗĶ1L·śĘųĪüŹÕ270kJČČĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£® | B£® | C£® | D£® |
ĶصēŅ»¶ĪŹ±¼äŗ󣬽Į°č¾łŌČ£¬ČÜŅŗµÄpHŌö“ó | ¼×µē¼«ÉĻµÄµē¼«·“Ó¦ĪŖ£ŗ 2Cl£ -2e£ = Cl2”ü | Ptµē¼«ÉĻµÄµē¼«·“Ó¦ĪŖ£ŗO2£«2H2O£«4e£==4OH£ | ×Ü·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ 2Fe3++Cu=Cu2++ 2Fe2+ |
|
|
|
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”³¤“ŗŹŠøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø¹²4·Ö£©ŌŚŅ»øö¹Ģ¶ØĢå»żĪŖ2ÉżµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė2molAŗĶ1molB£¬ ·¢ ÉśČēĻĀ·“Ó¦£ŗ 2A£Øg£©+B£Øg£© 3C£Øg£©+D£Øs£©£¬2·ÖÖÓ·“Ó¦“ļµ½Ę½ŗā£¬“ĖŹ±CµÄÅضČĪŖ1£®2 mol/L”£
3C£Øg£©+D£Øs£©£¬2·ÖÖÓ·“Ó¦“ļµ½Ę½ŗā£¬“ĖŹ±CµÄÅضČĪŖ1£®2 mol/L”£
£Ø1£©2·ÖÖÓÄŚÓĆB±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁ¶ČĪŖ £»
£Ø2£©ČōČŻĘ÷ĪĀ¶ČÉżøߣ¬Ę½ŗāŹ±»ģŗĻĘųĢåµÄĘ½¾łĻą¶ŌĦ¶ūÖŹĮæ¼õŠ”£¬ŌņÕż·“Ó¦ĪŖ£ŗ £ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©·“Ó¦”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014¼ŖĮÖŹ”°×³ĒŹŠø߶žÉĻŃ§ĘŚĘŚÄ©æ¼ŹŌ»Æѧ£ØB¾ķ£©ŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
³£ĪĀĻĀ£¬ĻĀĮŠĄė×ÓÄÜŹ¹“æĖ®ÖŠµÄH+Ąė×ÓŹżÄæŌö¼ÓµÄŹĒ£Ø £©
A£®S2£B£®CO32£C£®NH4+D£®Br£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com