
| A. | ①②③④⑤ | B. | 全部 | C. | ②④⑤⑦ | D. | ①④⑤⑦ |
分析 亚硫酸酸性小于HCl,所以二氧化硫和氯化钡溶液不反应,二氧化硫具有还原性,能被强氧化剂氧化为硫酸根离子,亚硫酸能和碱性气体生成亚硫酸盐,亚硫酸根离子能和氯化钡发生复分解反应,继续通入另一种气体却有沉淀产生,则该气体具有强氧化性或碱性,据此分析解答.
解答 解:亚硫酸酸性小于HCl,所以二氧化硫和氯化钡溶液不反应,二氧化硫具有还原性,能被强氧化剂氧化为硫酸根离子,亚硫酸能和碱性气体生成亚硫酸盐,亚硫酸根离子能和氯化钡发生复分解反应,继续通入另一种气体却有沉淀产生,则该气体具有强氧化性或碱性,
氨气属于碱性气体,氯气、臭氧、二氧化氮的水溶液硝酸都具有强氧化性,所以这几种气体符合条件,
故选C.
点评 本题考查物质之间的反应,明确二氧化硫性质是解本题关键,注意二氧化硫和氯化钡不反应,易错选项是氨气,题目难度不大.


科目:高中化学 来源: 题型:选择题
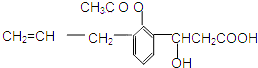
| A. | 可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 | |
| B. | 该物质1mol与足量NaOH溶液反应,消耗NaOH的物质的量为2mol | |
| C. | 可与氯化铁溶液发生显色反应 | |
| D. | 该有机物属于芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
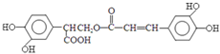
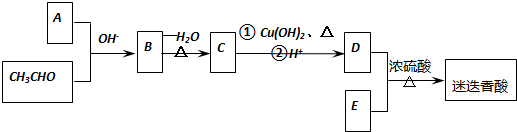
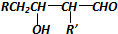 $→_{-H_{2}O}^{△}$
$→_{-H_{2}O}^{△}$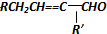
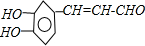 .
.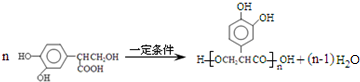 .
.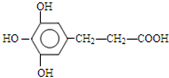 、
、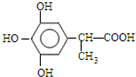 、
、 、
、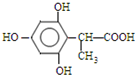 (任一种).
(任一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 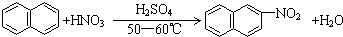 | |
| B. | CH3CH2CH2CHOHCH3$→_{△}^{浓硫酸}$CH3CH2CH=CHCH3+H2O | |
| C. | 2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2OCH2CH3+H2O | |
| D. | CH3COOH+CH3OH $→_{△}^{浓H_{2}SO_{4}}$ CH3COOCH3+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
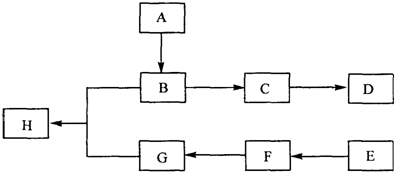
 ;
;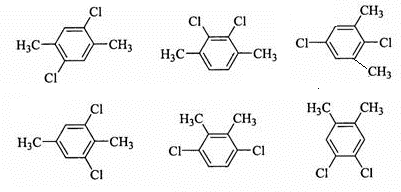 (其中两种)(任意两种)
(其中两种)(任意两种)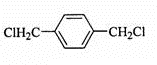
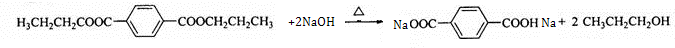 ,该反应的反应类型是取代反应.
,该反应的反应类型是取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有CO2和SO2 | B. | 可能有HBr、CO2 | ||
| C. | 肯定没有HBr、H2S、HCl | D. | 以上结论均不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
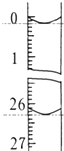 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.15 |
| 第二次 | 25.00 | 0.56 | 30.30 |
| 第三次 | 25.00 | 0.20 | 26.35 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v=0.10 mol•L-1•s-1是指1 s内某物质的物质的量浓度为0.10 mol•L-1 | |
| B. | 对于任何化学反应来说,反应速率越快,反应现象就越明显 | |
| C. | 化学反应速率只是对可逆反应才适用 | |
| D. | 根据反应速率的大小,可以知道反应进行的相对快慢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com