
【题目】有机物G是一种药物中间体,合成 G的部分流程如下:
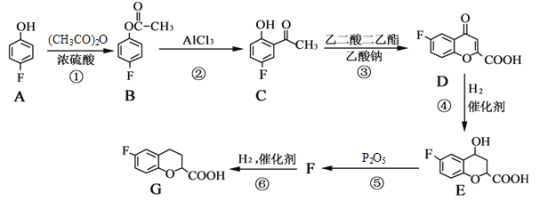
请回答下列问题:
(1)G物质中的含氧官能团的名称是___________、____________。
(2)上述⑤变化过程的反应类型是_____________。
(3)反应A→B的化学方程式为________________________________________。
(4)写出满足下列条件的C的同分异构体的结构简式:_______________________。
Ⅰ. 苯环上只有两种取代基。
Ⅱ. 分子中只有4种不同化学环境的氢。
Ⅲ. 能与NaHCO3反应生成CO2。
(5)根据已有知识并结合相关信息,写出以![]() 和乙酸酐为原料制备
和乙酸酐为原料制备![]() 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH__________
CH3CH2OH__________
【答案】羧基 醚键 消去反应 
![]()

【解析】
依据合成反应流程图,比较反应物、生成物结构的变化,判断反应类型,书写有关反应的化学方程式;根据要求写出符合题意的同分异构体;应用所学知识、流程中的信息,设计并写出合成反应流程图。
(1)物质G中含氧官能团羧基、醚键。
(2)从E→G,必有消去反应失去羟基,但G中无碳碳双键,又有与氢气加成反应。故反应⑤为消去反应,反应⑥为加成反应(或还原反应)。
(3)比较A、B结构简式可知,A中酚羟基氢被乙酰基(CH3CO-)取代,则反应①的化学方程式为 。
。
(4)能与NaHCO3反应生成CO2,则分子中有羧基(-COOH);苯环上的两个取代基可能是-COOH和-CH2F,或-CH2COOH和-F;取代基已有两种不同化学环境的氢原子,则苯环上有两种不同化学环境的氢原子,两种不同取代基应在苯环上对位。符合题意的C的同分异构体为![]() 。
。
(5)由于原料![]() 和乙酸酐可依次发生流程中的反应①②,先后生成
和乙酸酐可依次发生流程中的反应①②,先后生成 、
、 ;目标产物
;目标产物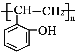 应是
应是 加聚反应生成;
加聚反应生成; 经与氢气加成、再与浓硫酸共热或与P2O5作用脱水可得
经与氢气加成、再与浓硫酸共热或与P2O5作用脱水可得 。故合成路线流程图如下:
。故合成路线流程图如下:



 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】下表列出了有关晶体的知识其中错误的是( )
A | B | C | D | |
晶体 | 硫化钾 | 干冰 | 金刚石 | 碘 |
组成晶体的微粒 | 阴阳离子 | 分子 | 原子 | 分子 |
晶体微粒间存在的作用力 | 离子键 | 共价键 | 共价键 | 范德华力 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。
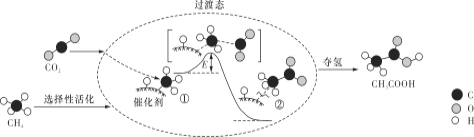
下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,七种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
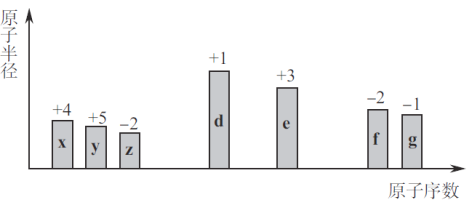
根据判断出的元素回答:
(1)x在元索周期表的位置是________________________。
(2)y的最高价氧化物对应的水化物与其氢化物反应,产物中含有化学键的类型为________________。
(3)d的单质在空气中充分燃烧,所得产物的电子式为________;7.8g该产物与足量的水完全反应,转移电子的数目为____________________。
(4)z、e、f的简单离子半径由大到小的顺序为_______________(用离子符号表示)。
(5)能说明g的非金属性比f强的实验事实是________________(列举一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某酸碱指示剂是一种有机弱酸,其在水溶液中的电离平衡与其呈现颜色相关:HIn(红色)H++In-(黄色),若向含此指示剂的溶液中加入盐酸,溶液将呈___色。
(2)下表列出了生产1 m3塑料的能耗和可从同量塑料回收的能量。
塑料 | 能耗/ kJ | 可回收能量/ kJ | 塑料 | 能耗/ kJ | 可回收能量/ kJ |
耐纶 | 7.8×104 | 4.2×104 | 丙烯酸类塑料 | 4.3×104 | 1.8×104 |
聚氯乙烯 | 3.8×104 | 1.6×104 | 聚丙烯 | 2.0×104 | 1.5×104 |
现废品收购站已回收如下数量的废塑料:耐纶5 m3、聚氯乙烯50 m3、丙烯酸类塑料5 m3、聚丙烯40 m3,如将它们加工成燃料,可回收能量______________ kJ。
(3)在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)zC(g);平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30mol/L。下列有关判断正确的(____)。
A.x+y<z B.平衡向正反应方向移动 C.B的转化率降低 D.C的体积分数增大
(4)2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3+Cl2PCl5.达平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是(____)
A.0.40mol B.0.20mol C.小于0.20mol D.大于0.20mol,小于0.40mol
(5)为了研究土壤的酸碱性,某学生做了如下实验:将一定体积的蒸馏水加入一定质量的土壤中,充分搅拌后,过滤并留取滤液,测滤液的pH后向滤液中滴加氨水,每加入2mL氨水就搅拌均匀并测量溶液的pH,所得实验记录如下:
加氨水体积 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
溶液的pH | 4 | 4 | 4 | 4 | 6 | 8 | 10 | 10 | 10 |
利用上述记录的数据,回答下列问题:
①所测土壤的酸碱性如何?_________(填酸性或者碱性)
②)所用氨水的c(OH—)为______________,
③为使该滤液呈中性,所加入氨水的恰当体积是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,科学家最近发现了一种新原子,它的原子核内有162个中子,质量数274,该元素的核电荷数为( )
A. 112 B. 161 C. 272 D. 433
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如右图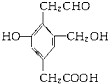 ,若等物质的量的该有机物分别与足量的Na、NaOH、Na2CO3、NaHCO3反应时,则消耗Na、NaOH、Na2CO3、NaHCO3的物质的量之比是( )
,若等物质的量的该有机物分别与足量的Na、NaOH、Na2CO3、NaHCO3反应时,则消耗Na、NaOH、Na2CO3、NaHCO3的物质的量之比是( )
A. 3 :2 :1 :1 B. 3 :3 :2 :1
C. 2 :2 :1:1 D. 3:2:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:

下列叙述错误的是
A. 合理处理废旧电池有利于保护环境和资源再利用
B. 从“正极片”中可回收的金属元素有Al、Fe、Li、C
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用硫酸钠代替碳酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求完成下列各项填空:
(1)AlCl3的水溶液呈_______(填“酸”、“中”或“碱”)性,常温时的pH_____7(填“>”、“<”或“=”),原因是(用离子方程式表示):_________________________;实验室在配制 AlCl3溶液时,常将 AlCl3固体先溶于浓盐酸中,然后再用蒸馏水稀释到所需的浓度,以_________(填“促进”或“抑制”)其水解。将AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是________________(填化学式)。
(2)在纯碱溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的氯化钡溶液,所观察到的现象是___________________________________________,其原因是(以离子方程式和简要的文字说明):_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com