
 X��Y��W��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ��������������ͼ��ʾ����֪X��һ�ֺ��ص�������Ϊ18��������Ϊ10��Y��Neԭ�ӵĺ�������������1��W�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ķǽ�������ͬ��������Ԫ������ǿ��
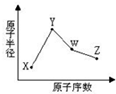
X��Y��W��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ��������������ͼ��ʾ����֪X��һ�ֺ��ص�������Ϊ18��������Ϊ10��Y��Neԭ�ӵĺ�������������1��W�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ķǽ�������ͬ��������Ԫ������ǿ��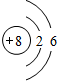 ��
������ X��Y��W��Z�����ֳ����Ķ�����Ԫ�أ���֪X��һ�ֺ��ص�������Ϊ18��������Ϊ10����XԪ��ԭ�ӵ�������Ϊ18-10=8����XΪ��Ԫ�أ�Y��Neԭ�ӵĺ�����������1��XΪNa��F��Xԭ�Ӱ뾶������ԭ�ӣ���XΪNaԪ�أ�W�ĵ�����һ�ֳ����İ뵼����ϣ�ԭ����������NaԪ�أ���WΪSiԪ�أ�Z���������ӵ�������ͬ��������Ԫ�������ԭ����������Si����ZΪClԪ�أ��Դ˽����⣮
��� �⣺X��Y��W��Z�����ֳ����Ķ�����Ԫ�أ���֪X��һ�ֺ��ص�������Ϊ18��������Ϊ10����XԪ��ԭ�ӵ�������Ϊ18-10=8����XΪ��Ԫ�أ�Y��Neԭ�ӵĺ�����������1��XΪNa��F��Xԭ�Ӱ뾶������ԭ�ӣ���XΪNaԪ�أ�W�ĵ�����һ�ֳ����İ뵼����ϣ�ԭ����������NaԪ�أ���WΪSiԪ�أ�Z���������ӵ�������ͬ��������Ԫ�������ԭ����������Si����ZΪClԪ�أ�
��1��WΪSi��ԭ�Ӻ��������Ϊ14����3�����Ӳ㣬����������Ϊ4���������ڱ��е�������IVA�壬XΪO�������ӵĽṹʾ��ͼΪ��
�ʴ�Ϊ������IVA��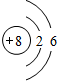 ��
��
��2��ZΪClԪ�أ�����Ԫ�صķǽ�����Cl��Br�����⻯���ȶ���HCl��HBr�����ȶ�����HCl��������HF����֮���������������˷���֮������������������ʵ��۷е�ϸߵ���HF���ʴ�Ϊ��HCl��HF��
��3��ͬ������ԭ����������ԭ�Ӱ뾶��С��ԭ��ʧȥ���ӵ�����������Ԫ�صĽ��������������Խ�����Na��Mg��Ԫ�صĽ�����Խǿ���䵥����ˮ�����û���������Խ���ף����Կ���ͨ��Na����ˮ���ҷ�Ӧ����Mg����ˮ��Ӧ����֤��Ԫ�صĽ�����Na��Mg���ʴ�Ϊ��Na��Na����ˮ���ҷ�Ӧ����Mg����ˮ��Ӧ������
��4��Y������������Ӧ��ˮ����NaOH��ǿ�Z������������Ӧ��ˮ����HClO4��һԪǿ�ᣬ���߷�������кͷ�Ӧ�������������ƺ�ˮ��������Ӧ�Ļ�ѧ��Ӧ����ʽ��NaOH+HClO4=NaClO4+H2O��
�ʴ�Ϊ��NaOH+HClO4=NaClO4+H2O��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ����Ŀ�Ѷ��еȣ�ע�����Ԫ�������ɵĵݱ�����Լ�ԭ�Ӻ�����ӵ��Ų��ص㣬��ȷԪ�ص�����Ϊ������Ĺؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�����ϵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
ijͬѧ�������ͼ��ʾװ���������ô�������ijŨ��ϡ���ᷴӦ��ȡNO���塣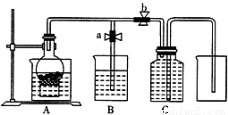
��1��������a���رտ���bʱ��A�и�����й۲쵽��ʵ�������� ���ձ�B��ʢ���� ��Һ���� ʱ�رտ���a������b����ʱC������ˮ���ռ�NO���塣��C����������رտ���b��װ��A�й۲쵽�������Ǣ� ���� ��
��2����a mol Fe�뺬b mol HNO3��ϡ��Һ��ַ�Ӧ��������Ļ�ԭ ����ֻ��NO�������۷����ձ�A�������Һ����Ҫ��������ɼ������ʵ���������������±�δ��ɵĿո��С�
����ֻ��NO�������۷����ձ�A�������Һ����Ҫ��������ɼ������ʵ���������������±�δ��ɵĿո��С�
a/bȡֵ��Χ | ������Һ�е���Ҫ�����Ӽ������ʵ��� |
<1/4 | |
=1/4 | a mol Fe3+ |
����1/4��3/8 | |
=3/8 | a mol Fe2+ |
>3/8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ��ˮ | C�� | ̼������Һ | D�� | ��̪�Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
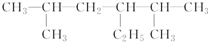 ��������2��5-����-3-�һ����飬�����ʵ�һ�ȴ�����8�֣�
��������2��5-����-3-�һ����飬�����ʵ�һ�ȴ�����8�֣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ˮ���γ������������壬����������ˮ��ɱ������ | |
| B�� | �����û����������е����������ڸ�����ҵ�д���ұ���� | |
| C�� | ̼���ƾ��м��ԣ�������θ���кͼ� | |
| D�� | ����þ�۵�ߣ����������²��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
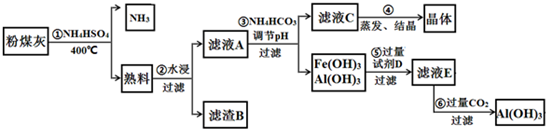
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£��������CH4��CO2��������� | |
| B�� | ��NaOH��Һ��ϡ���ᷴӦ����������H2���������۵�������� | |
| C�� | �����£�ͭ��Ũ����Ѹ�ٷ�Ӧ����SO2���� | |
| D�� | 1mol OH-��17g NH3�����ĵ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��NH3��=$\frac{2}{3}$v��H2O�� | B�� | v��O2��=$\frac{6}{5}$v��H2O�� | C�� | v��NH3��=$\frac{5}{4}$v��O2�� | D�� | v��O2��=$\frac{4}{5}$v��NO�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | K+ | B�� | Ba2+ | C�� | Zn2+ | D�� | Mg2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com