
| A. | 碳氢键 | B. | 碳碳键 | C. | 氢氧键 | D. | 碳氧单键 |
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 强电解质 | HBr | FeCl3 | H2SO4 | Ca(OH)2 |
| 弱电解质 | HF | HCOOH | BaSO4 | HI |
| 非电解质 | NH3 | Cu | H2O | C2H5OH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
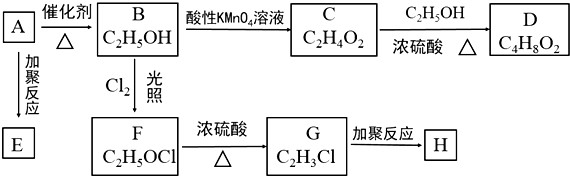
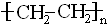 ;
; CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醛 | B. | 乙醇 | C. | 乙二醇 | D. | 乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.根据图示晶胞结构,推算晶体中Y、Ba、Cu和O原子个数比,确定其化学式为YBa2Cu3O7.
钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.根据图示晶胞结构,推算晶体中Y、Ba、Cu和O原子个数比,确定其化学式为YBa2Cu3O7.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点高,有滑腻感,可用于制润滑剂 | |
| B. | 质软,在纸上划过留痕迹,可用于制铅笔芯 | |
| C. | 有良好的导电性,可用于制干电池的电极 | |
| D. | 耐高温,可用于制作刻划玻璃的工具 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com