
| 物质 | 结构 | 某些性质 |
| 草酸 | 分子式:H2C2O4•2H2O | 无色,易溶于水;其钠盐和钾盐易溶于水,钙盐难溶于水 |
| 结构简式:HOOC-COOH | 熔点:101℃;升华温度:125℃;170℃以上分解 |
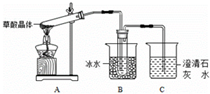
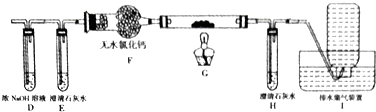
分析 (1)草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,如果草酸受热分解,分解时会产生二氧化碳而使澄清石灰水变浑浊;草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水,B装置温度较低,有冷凝作用,防止干扰实验,装置C中可能发生二氧化碳和氢氧化钙反应、草酸和氢氧化钙反应;
(2)①要检验生成CO,在甲组实验后,用浓氢氧化钠除去二氧化碳,用澄清石灰水检验二氧化碳,用无水氯化钙干燥CO,利用CO的还原性将CO氧化,再利用澄清石灰水检验生成的二氧化碳,用排水法收集CO;所以装置E和H中的澄清石灰水的作用分别是验证二氧化碳是否除完、证明产物中含有一氧化碳,装置G反应管中盛有的固体物质是氧化铜(CuO);
②CO具有还原性,其氧化产物是二氧化碳,二氧化碳能使澄清石灰水变浑浊.
解答 解:(1)草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,如果草酸受热分解,分解时会产生二氧化碳,二氧化碳和氢氧化钙反应生成难溶性的碳酸钙沉淀而使澄清石灰水变浑浊,所以C中观察到的现象是:装置C中可观察到的现象是①导管口有气泡出现 ②石灰水变浑浊,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水,草酸易挥发,导致生成的气体中含有草酸,草酸和氢氧化钙反应生成难溶性的草酸钙而干扰二氧化碳的检验,B装置温度较低,有冷凝作用,防止干扰二氧化碳的检验,装置C中可能发生二氧化碳和氢氧化钙反应:CO2+Ca(OH)2=CaCO3↓+H2O、草酸和氢氧化钙反应:H2C2O4+Ca(OH)2=CaC2O4↓+H2O,
故答案为:CO2;冷凝(水蒸气、草酸),避免草酸进入装置C反应生成沉淀,干扰CO2的检验;CO2+Ca(OH)2=CaCO3↓+H2O;H2C2O4+Ca(OH)2=CaC2O4↓+H2O;
(2)①要检验生成CO,在甲组实验后,用浓氢氧化钠除去二氧化碳,用澄清石灰水检验二氧化碳,用无水氯化钙干燥CO,H装置中盛放的物质应该具有氧化性,且和CO反应有明显现象发生,CuO能被CO还原且反应过程中黑色固体变为红色,现象明显,所以H中盛放的物质是CuO,利用CO和CuO发生还原反应生成CO2,再利用澄清石灰水检验生成的二氧化碳,用排水法收集CO避免环境污染,
故答案为:验证二氧化碳是否除完;证明产物中含有一氧化碳;氧化铜(CuO);CO;
②CO具有还原性,其氧化产物是二氧化碳,二氧化碳能使澄清石灰水变浑浊,且CO将黑色的CuO还原为红色的Cu,只要H中黑色固体转化为红色且其后的D装置溶液变浑浊就说明含有CO,
故答案为:H中的粉末由黑色变为红色,D中澄清石灰水变浑浊.
点评 本题考查草酸的性质探究实验方案设计,侧重考查学生知识综合应用、实验基本操作能力及实验方案设计能力,综合性较强,为高频考点,掌握草酸的性质以及实验原理是解答关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
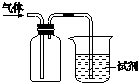
| A. | 该装置可用于收集NO2,试剂为水,用于吸收多余的NO2 | |
| B. | 若试剂是紫色石蕊试液,通入Cl2,溶液先变红后褪色,则氯气有漂白性 | |
| C. | 该装置可用于收集NH3,试剂为水,用于吸收多余的NH3 | |
| D. | 若试剂是酸性KMnO4溶液,通入SO2,溶液褪色,则得出SO2有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度不再随时间变化 | |
| B. | 容器内X、Y、Z的浓度之比为:1:2:2 | |
| C. | 单位时间消耗0.1molX,同时生成0.2molY | |
| D. | 单位时间消耗0.1molX,同时生成0.2molZ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、 .
. .
. 、
、 .
. 、
、
 +
+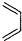 $\stackrel{△}{→}$
$\stackrel{△}{→}$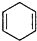 ,如果要合成
,如果要合成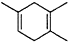 所用的原始原料可以是AC
所用的原始原料可以是AC查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:Na>Al | B. | 热稳定性NaHCO3>Na2CO3 | ||
| C. | 酸性:H2CO3>H2SiO3 | D. | 氧化性Br2>Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氯水,再加入KSCN溶液,溶液显红色,则溶液中一定含有Fe2+ | |
| B. | 加入盐酸,产生无色无味且能使澄清石灰水变浑浊的气体,则溶液中一定含有CO32- | |
| C. | 加入Ba(NO3)2溶液,再加入稀盐酸,产生白色沉淀,则溶液中一定含有SO42- | |
| D. | 加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,则溶液中一定含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量 | B. | 原子总数 | C. | 密度 | D. | 分子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体是一种混合物 | B. | 胶体粒子有颜色 | ||
| C. | 胶体粒子直径在1-100nm之间 | D. | 光束通过胶体时有丁达尔效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com