
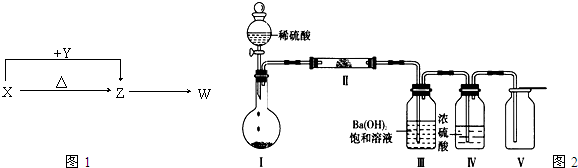
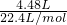 =0.2mol,n(NaOH)=0.3mol,发生2CO2+3NaOH=Na2CO3+NaHCO3+H2O,生成物为Na2CO3和NaHCO3,
=0.2mol,n(NaOH)=0.3mol,发生2CO2+3NaOH=Na2CO3+NaHCO3+H2O,生成物为Na2CO3和NaHCO3, 2H2O+O2↑进行,所需仪器装置是Ⅰ、Ⅳ、Ⅴ,故答案为:H2O2;Ⅰ、Ⅳ、Ⅴ.
2H2O+O2↑进行,所需仪器装置是Ⅰ、Ⅳ、Ⅴ,故答案为:H2O2;Ⅰ、Ⅳ、Ⅴ.

科目:高中化学 来源: 题型:阅读理解
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相同 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
查看答案和解析>>
科目:高中化学 来源:2014届安徽省高三上学期第一次联考化学试卷(解析版) 题型:选择题
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
啤酒和饮料中常溶有X的最高价氧化物,打开瓶子时,这种氧化物会大量逸出 |
|
Y |
Y2是空气中含量最高的气体单质 |
|
Z |
Z的基态原子最外层电子排布式为2s22p4 |
|
W |
W的一种核素质量数为27,中子数为14 |
(1)W位于元素周期表第 周期第 族;Z和W的最简单的离子半径大小关系为
(用离子符号表示)
(2)一种X形成的单质,是自然界硬度最大的物质,若熔化这种单质,所需克服的微粒间的作用力是 ;Y的电负性比Z (填“大”或“小”)
(3)W的单质与NaOH溶液反应的离子方程式为 , W在高温条件下可还原高熔点的金属氧化物制的金属单质,写出W还原Cr2O3反应的化学方程式: 。
(4)煤燃烧产生的烟气中有Y的氧化物,会引起严重的环境问题,因此,常用XH4催化还原以消除污染,已知:
XH4(g)+2 YO2(g)== Y2(g)+ XO2(g)+2H2O (g) △H1= -867kJ/mol
2 YO2(g)  Y2O4(g)
△H2=-56.9kJ/mol
Y2O4(g)
△H2=-56.9kJ/mol
查看答案和解析>>
科目:高中化学 来源:2013届河南周口重点高中四校高二下学期第一次联考化学卷(解析版) 题型:推断题
(11分)X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
|
Z |
Z和Y同周期,Z的电负性大于Y |
|
W |
W的一种核素的质量数为63,中子数为34 |
(1)Y的元素符号是
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键,中心原子杂化轨道类型 ;在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子核外电子排布式是 。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。此反应的化学方程式是 。
(5)请设计一个实验方案,比较Y、Z单质氧化性的强弱:
_____________________________________________________________________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com