
| H2O/H+ |
 ������HΪ
������HΪ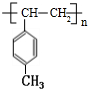 ��
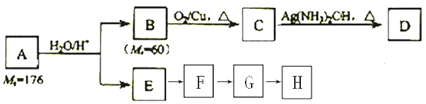
��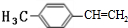 ��G�����Ӿ۷�Ӧ�õ��߾���H������ϩ����A��̼��ԭ����Ŀ��Ϊ3��4������Է�������Ϊ176���ṹB��G�Ľṹ����Ϣ��֪��AΪ
��G�����Ӿ۷�Ӧ�õ��߾���H������ϩ����A��̼��ԭ����Ŀ��Ϊ3��4������Է�������Ϊ176���ṹB��G�Ľṹ����Ϣ��֪��AΪ ����EΪ
����EΪ �������������ӳɷ�Ӧ����FΪ
�������������ӳɷ�Ӧ����FΪ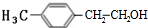 ��F��Ũ���ᡢ���������·�����ȥ��Ӧ����G���ݴ˽��
��F��Ũ���ᡢ���������·�����ȥ��Ӧ����G���ݴ˽�� ��G�����Ӿ۷�Ӧ�õ��߾���H������ϩ����A��̼��ԭ����Ŀ��Ϊ3��4������Է�������Ϊ176���ṹB��G�Ľṹ����Ϣ��֪��AΪ
��G�����Ӿ۷�Ӧ�õ��߾���H������ϩ����A��̼��ԭ����Ŀ��Ϊ3��4������Է�������Ϊ176���ṹB��G�Ľṹ����Ϣ��֪��AΪ ����EΪ
����EΪ �������������ӳɷ�Ӧ����FΪ
�������������ӳɷ�Ӧ����FΪ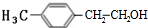 ��F��Ũ���ᡢ���������·�����ȥ��Ӧ����G��
��F��Ũ���ᡢ���������·�����ȥ��Ӧ����G�� ��BΪCH3CH2CH2OH������Ϊ1-�������ʴ�Ϊ��
��BΪCH3CH2CH2OH������Ϊ1-�������ʴ�Ϊ�� ��1-������
��1-������| �� |

| һ������ |
 ��
��| �� |

| һ������ |
 ��
�� ����ͬ���칹�����������
����ͬ���칹����������� ��
�� ��
�� ��
�� ��
�� ��
�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��Ӧʱ��/min | n��CO��/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
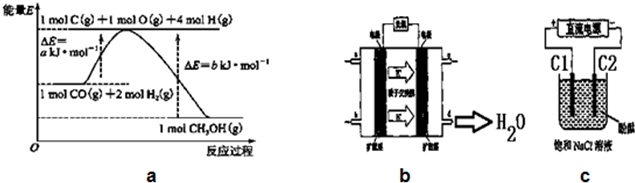
A����Ӧ��t1 min�ڵ�ƽ������Ϊv(H2)=
| ||
| B�����������������䣬��ʼʱ�������г���0.60molCO��1.20molH2O������ƽ��ʱ��n��CO2��=0.40mol | ||
| C�����������������䣬��ƽ����ϵ����ͨ��0.20molH2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCOת��������H2O������������� | ||
| D���¶�����800��ʱ����������Ӧƽ�ⳣ��Ϊ0.64��������ӦΪ���ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ŵ� |
| ��� |
| A����صĵ��ҺΪ������Һ������ΪNi2O3������ΪFe |
| B����طŵ�ʱ��������ӦΪFe+2OH--2e-=Fe��OH��2 |
| C����س������У�����������Һ��pH���� |
| D����س��ʱ��������ӦΪ2Ni��OH��2+2OH--2e-=Ni2O3+3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
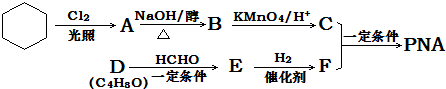
| KMnO4/H+ |
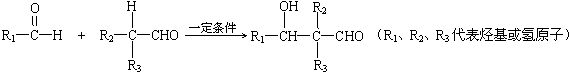
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ��Ũ�ȣ�mol/L���¶� | 10min | 20min | 30min | 40min | 50min | 60min |
| 300�� | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500�� | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
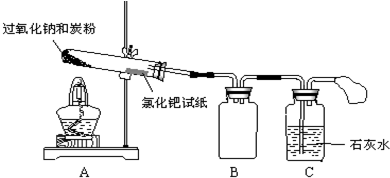
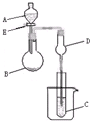 һ��װ���ж�����;�ǻ�ѧʵ���о������ֵ����⣮��ͼ��ʾװ�ý���ʵ�飬��A��μ���B�У�
һ��װ���ж�����;�ǻ�ѧʵ���о������ֵ����⣮��ͼ��ʾװ�ý���ʵ�飬��A��μ���B�У��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com