
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 |  |
| ② | 往试管Ⅰ中加入FeCl2溶液后,加入2滴KSCN溶液并振荡 | 无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管Ⅱ中加入3%H2O2溶液并振荡 | 溶液变蓝 | 证明以I-形式存在 |
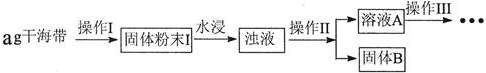
分析 干海带灼烧得到固体粉末Ⅰ,水浸后得到浊液,操作Ⅱ是过滤得到溶液A,操作Ⅲ是将上述溶液稀释配制成200mL溶液,用高锰酸钾溶液氧化得到碘单质,用硫代硫酸钠吸收碘单质测定碘的含量,
(1)依据流程图分析,操作Ⅰ固体灼烧在坩埚中;操作Ⅱ是分离固体和液体的实验操作过滤;
(2)加热使含碘物质更多地溶解于水溶液中;
(3)②利用亚铁离子具有还原性,碘酸根离子在酸性溶液中具有氧化性,检验是否含有铁离子;
③利用试剂过氧化氢具有氧化性可以氧化碘离子为碘单质,遇到淀粉变蓝;
(4)依据A溶液中碘离子被高锰酸钾溶液氧化为碘单质,碘单质被硫代硫酸钠溶液还原为碘离子,中和滴定过程中,到蓝色恰好褪去不再变化证明反应到终点;依据离子方程式计算得到碘 元素含量.
解答 解:(1)流程图分析,操作Ⅰ固体灼烧在坩埚中;操作Ⅱ是分离固体和液体的实验操作过滤,
故答案为:坩埚;过滤;
(2)水浸要将悬浊液煮沸2-3min是为了增大含碘物质的溶解度,使更多的含碘物质溶解,
故答案为:加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液;
(3)②利用亚铁离子具有还原性,碘酸根离子在酸性溶液中具有氧化性,检验是否含有铁离子,往试管I中加入氯化亚铁溶液,后加入2滴KSCN溶液并振荡,无血红色出现证明不是以IO3-形式存在;
故答案为:FeCl2溶液,后加入2滴KSCN溶液并振荡;
③往试管II中加入3%过氧化氢具有氧化性可以氧化碘离子为碘单质,遇到淀粉变蓝,
故答案为:3% H2O2溶液并振荡;溶液变蓝;
(4)A溶液中碘离子被高锰酸钾溶液氧化为碘单质,碘单质被硫代硫酸钠溶液还原为碘离子,中和滴定过程中,到蓝色恰好褪去不再变化证明反应到终点;设碘离子物质的量为x,
2I-~I2~2Na2S2O3
2 2
x 0.01mol/L×V×10-3L
x=V×10-5mol
200ml溶液中含碘元素物质的量为=V×10-4mol
海带中碘元素的百分含量=$\frac{V×1{0}^{-4}×127g/mol}{ag}$×100%=$\frac{1.27V}{a}$×100%,
故答案为:溶液蓝色刚好褪去,30s内不恢复蓝色,$\frac{1.27V}{a}$×100%.
点评 本题考查了物质制备的流程分析判断,实验方案的设计原则和步骤,滴定实验的计算应用,反应现象和物质性质是解题关键,题目难度中等.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应不一定是吸热反应 | |
| B. | 任何放热反应在常温条件下一定能够发生 | |
| C. | 反应物和生成物具有的总能量决定了反应是吸热还是放热 | |
| D. | 吸热反应在一定条件下(如加热等)也能够发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
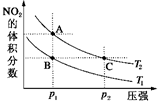 反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.正确的是( )| A. | A、C两点的反应速率:A>C | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | A、C两点气体的平均相对分子质量:A>C | |
| D. | 由状态B到状态A,可以用加热的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③① | B. | ③② | C. | ②①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸滴在石灰石上:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 少量CO2通入NaOH溶液中,:CO2+2OH-═CO32-+H2O | |
| C. | NaOH溶液和KHSO4溶液反应:OH-+H+═H2O | |
| D. | Na2O溶于稀盐酸:O2-+2H+═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com