
| A. | 每消耗1molCH4可以向外电路提供4mole- | |
| B. | 负极上CH4失去电子,电极反应式为:CH4+10OH--8e-=CO32-+7H2O | |
| C. | 正极上O2得到电子,电极反应式为:O2+4H++4e-=2H2O | |
| D. | 电池放电后,溶液pH不断升高 |
分析 碱性甲烷燃料电池,具有还原性的甲烷为原电池的负极,发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O,通入氧气的一极为原电池的正极,发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,原电池工作时,电子从负极经外电路流向正极,电解质溶液中,阳离子向正极移动,阴离子向负极移动.
解答 解:A、通入CH4的电极为负极,电极反应为:CH4+10OH--8e-=CO32-+7H2O,每消耗1molCH4可以向外电路提供8mole-,故A错误;
B、通入CH4的电极为负极失电子反应氧化反应,电极反应为CH4+10OH--8e-=CO32-+7H2O,故B正确;
C、通入氧气的一极为原电池的正极,得到电子发生还原反应:O2+2H2O+4e-=4OH-,故C错误;
D、电池反应式为:CH4+2OH-+2O2=CO32-+3H2O,随着反应的进行,溶液中氢氧根离子不断减少,溶液pH不断减小,所以该电池使用一段时间后应补充KOH,故D错误;
故选B.
点评 本题考查碱性甲烷电池的工作原理,题目难度不大,本题中注意把握电极反应式的书写,正确判断两极的化学反应,在学习中注意积累电子、电流、离子的流向.


科目:高中化学 来源: 题型:解答题

 +NaHCO3→
+NaHCO3→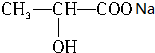 +CO2↑+H2O
+CO2↑+H2O $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
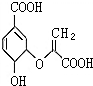 分支酸在植物的芳香族氨基酸的合成系统中作为中间体,其结构简式如图.下列关于分支酸的叙述正确的是( )
分支酸在植物的芳香族氨基酸的合成系统中作为中间体,其结构简式如图.下列关于分支酸的叙述正确的是( )| A. | 分支酸属于芳香族化合物 | |
| B. | 遇氯化铁溶液发生显色反应,可用于检验分支酸 | |
| C. | 1 mol分支酸最多可与3molH2发生加成反应 | |
| D. | 1 mol分支酸与足量NaHCO3溶液反应放出67.2L二氧化碳气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓氨水滴进碱石灰里可制得氨气 | |
| B. | 蘸浓氨水和蘸浓硫酸的玻璃棒靠近会冒白烟 | |
| C. | 锌片与稀硝酸反应可制得氢气 | |
| D. | 铜片与浓硝酸反应可制得一氧化氮 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com