
据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源,下列所列能源不是清洁能源的是
A. 太阳能 B. 石油 C. 天然气 D. 酒精
科目:高中化学 来源: 题型:
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
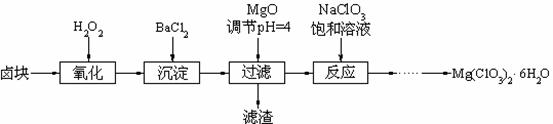
已知:
①卤块主要成分为MgCl2·6H2O,含有MgSO4、
FeCl2等杂质。
 ②几种化合物的溶解度(S)随温度(T)变化曲线
②几种化合物的溶解度(S)随温度(T)变化曲线
如右图。
40.加MgO后过滤所得滤渣的主要成分为 。
41.加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全? 。
42.加入NaClO3饱和溶液会发生如下反应:
MgCl2+2NaClO3 Mg(ClO3)2+2NaCl↓,
Mg(ClO3)2+2NaCl↓,
请利用该反应,结合右图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应,② ;③ ;④ ;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50g产品溶解定容成100mL溶液。
步骤2:取10mL于锥形瓶中,加入10mL稀硫酸和20mL1.000mol/L的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol/LK2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+ 2Cr3++6Fe3++7H2O。
2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL。
43.上述产品测定中需要检查是否漏液的仪器有 。
步骤3中若滴定前不用标准液润洗滴定管,会导致最终结果偏 。(填“大”或“小”)。
44.产品中Mg(ClO3) 2·6H2O的质量分数为 。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
发展低碳经济,构建低碳社会。科学家们提出利用以工业废气中的CO2为原料,以CuO与ZnO混合物为催化剂,其反应为:CO2 + 3H2 CH3OH + H2O。
CH3OH + H2O。
(1)某温度下,在体积为l L的密闭容器中充入lmol CO2和4mol H2,测得CO2和CH3OH(g)的浓度随时间变化如(Ⅰ)图所示。


从反应开始到平衡,甲醇的平均反应速率v(CH3OH)= ;氢气的转化率为 。
(2)常温常压下已知下列反应的能量变化如(Ⅱ)图所示:


写出由二氧化碳和氢气制备甲醇的热化学方程式: ,该反应的△S 0(填“>”或“<”或“=”);反应达到平衡后,要使该平衡向右移动,其它条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积 B.升高温度 C.恒容条件下通入CO2 D.使用合适的催化剂
(3)在实际生产中发现,随着甲醇的生成,还伴随有少量CO等副产物出现,且CO2的转化率、甲醇和CO的含量还受气体混合物在反应锅炉内的流动速率、催化剂CuO的质量分数影响。通过实验分别得到如下图。
 ①由图(Ⅲ)得,生产甲醇的气体最佳流动速率为 L·h-1;
①由图(Ⅲ)得,生产甲醇的气体最佳流动速率为 L·h-1;
②已知当催化剂中没有CuO,只有单组份ZnO时,反应速率最大。说明为什么不选择单组份ZnO的原因 ,根据图(Ⅳ)判断,催化剂CuO的质量分数最
好为 %。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下物质间的每步转化通过一步反应就能实现的是( )
A.Al--Al2O3--Al(OH)3--NaAlO2 B.Mg--MgCl2--Mg(OH)2—MgO
C.S--SO3-- H2SO4-- MgSO4 D.Si--SiO2--H2SiO3--Na2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
通常情况下,用到的下列反应试剂所发生的反应,能使反应物碳链缩短的是
A.氢氧化钠的水溶液 B.氢氧化铜碱性悬浊液
C.溴的四氯化碳溶液 D.氢气(镍作催化剂)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com