
【题目】按要求填空:
(1)有下列几种物质 A.金刚石和石墨 B. C2H4和C2H6 C. C2H6和C5H12
D. CH3CH2CH2CH3和CH3CH(CH3)2 E.35Cl和37Cl
①属于同位素的是_____,
②属于同素异形体的是_____,
③属于同系物的是_____,
④属于同分异构体的是_____;
(2)相对分子质量为72的某烃,
①则它的分子式是 _________,
②它存在多种结构,其沸点最低的结构简式是 ________。
【答案】E A C D C5H12 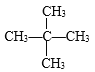
【解析】
(1)质子数相同中子数不同的原子互成同位素;
(2)由同一元素组成的不同性质的单质互为同素异形体;
(3)同系物是结构相似,在分子组成上相差一个或若干CH2原子团的化合物;
(4)同分异构体是分子式相同,结构不同的化合物。
(5)用商余法计算确定物质的分子式,然后根据同分异构体中,支链越多,物质的沸点越低确定物质的结构简式。
(1) A.金刚石和石墨是C元素的两种不同性质的单质,二者互为同素异形体; B.C2H4属于烯烃,而C2H6属于烷烃,二者不是同系物,也不是同分异构体;
C.C2H6和C5H12都是烷烃,二者互为同系物;
D.CH3CH2CH2CH3和CH3CH(CH3)2分子式相同,结构不同,二者互为同分异构体; E.35Cl和37Cl是Cl元素的两种原子,二者互为同位素。
故①属于同位素的是E;②属于同素异形体的是A;③属于同系物的是C;④属于同分异构体的是D;
(2)①相对分子质量为72的某烃其中含有的C原子数为C:72÷12=6,根据烃分子结构特点,1个C原子的相对原子质量与12个H原子相对原子质量相等,因此该物质分子为C5H12;
②它存在三种结构,CH3CH2CH2CH2CH3、![]() 、
、 ,对于同分异构体来说,物质分子中含有的支链越多,物质的分子之间距离越大,分子间作用力越小,物质的沸点就越低,故上述同分异构体中沸点最低的结构简式是
,对于同分异构体来说,物质分子中含有的支链越多,物质的分子之间距离越大,分子间作用力越小,物质的沸点就越低,故上述同分异构体中沸点最低的结构简式是 。
。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】以乙炔为主要原料可以合成聚氯乙烯、聚丙烯腈和氯丁橡胶,下图所示是有关合成路线图。
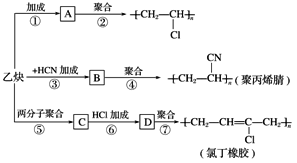
已知反应:
nCH2===CH—CH===CH2![]()
![]()
请完成下列各题:
(1)写出下列物质的结构简式:
A________________,C________________。
(2)写出下列反应的化学方程式:
反应②________________________________________________________________________;
反应③________________________________________________________________________;
反应⑥________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:

某化学兴趣小组同学模拟该流程设计了如下实验装置:

回答下列问题:
(1)a处可用来检验I中的反应是否发生,选用的试剂是______________,若要停止I中的化学反应,除停止加热外,还要采取的操作是________________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O ②可能是CuO;③可能是CuS;④_______。乙同学提出假设①一定不成立,该同学的依据是______;丙同学做了如下实验来验证黑色物质的组成:

基于上述假设分析,黑色物质的组成为__________________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________。
(4)为检验制得的硫代硫酸钠产品的纯度,该小组称取5.0g产品配成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:向锥形瓶中加入25.00mL 0.01mol·L-1的KIO3溶液,再加入过量的KI溶液并酸化,发生反应的离子方程式为___________,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应I2 + 2S2O32- == 2I- + S4O62-,当达到滴定终点时,消耗Na2S2O3溶液20.00mL,则该产品的纯度是____________(保留3个有效数字)。
(5)丁同学提出上述实验装置的设计存在不足,建议在I上__________;在I、II之间增加_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计下列方案对A盐的水解液进行鉴定:
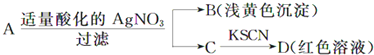
由此得出的结论中,不正确的是( )
A.D溶液中存在Fe(SCN)3 B.滤液中有Fe3+
C.B为AgBr D.A一定为无氧酸盐FeBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 0.1 mol·L-1 NH4C1溶液加蒸馏水稀释,溶液的pH不断减小
B. 常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
C. NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则[Na+]= 2[![]() ]
]
D. 0.1 mol·L-1的NaHA溶液,其pH=4时:[HA-]>[H+]>[H2A]>[A2-]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2S溶液中存在水解平衡:S2-+H2O![]() HS-+OH,在溶液中加入少量CuSO4固体,HS-浓度减小。下列说法正确的是
HS-+OH,在溶液中加入少量CuSO4固体,HS-浓度减小。下列说法正确的是
A. 稀释溶液,水解平衡常数增大
B. Ksp(CuS)<Ksp[Cu(OH)2]
C. 升高温度![]() 增大
增大
D. 加入MgCl2固体,HS-浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在紫外线的作用下,氧气可生成臭氧:3O2![]() 2O3,一定条件下该反应达到平衡状态的标志是( )
2O3,一定条件下该反应达到平衡状态的标志是( )
A. 单位时间内生成2 mol O3,同时消耗3 mol O2
B. O2的消耗速率0.3 mol·L-1·s-1,O3的消耗速率0.2 mol·L-1·s-1
C. 容器内,2种气体O3、O2浓度相等
D. 气体密度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应CO(g)+H2O(g)![]() CO 2(g)+ H 2(g) △H﹤0,在其他条件不变的情况下
CO 2(g)+ H 2(g) △H﹤0,在其他条件不变的情况下
A. 加入催化剂,改变了反应的途径,反应的△H也随之改变
B. 改变压强,平衡不发生移动,反应放出的热量不变
C. 升高温度,反应速率加快,反应放出的热量不变
D. 若在原电池中进行,反应放出的热量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com