
【题目】已知反应![]()
![]() ,起始加入量
,起始加入量![]() 为
为![]() ,
,![]() 为
为![]() ,HCOOH为
,HCOOH为![]() ,在一定温度下,不同时刻甲酸乙酯的物质的量如下:
,在一定温度下,不同时刻甲酸乙酯的物质的量如下:![]() 注:本题速率单位用
注:本题速率单位用![]() 表示
表示![]()
| 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 | 55 |
|
|
|
|
|
|
|
|
|
|
|
|
|
下列说法不正确的是 ![]()
![]()
A.以表中![]() 为单位,
为单位,![]() 内最大的平均反应速率在
内最大的平均反应速率在![]() 之间
之间
B.前![]() 甲酸乙酯的平均反应速率为
甲酸乙酯的平均反应速率为![]()
C.甲酸乙酯的反应速率先增大后减小的原因是该反应放热
D.开始时若加适量的NaOH,也可以加快甲酸乙酯水解速率
科目:高中化学 来源: 题型:
【题目】(1)按要求写出电子式:CO2_________ COCl2_________ NaCN______ N2H![]() _______
_______
(2)元素周期表中“对角线规则”是指处于周期表中对角线位置(左上和右下方)的两元素,其性质具有相似性,例如:Be和Al处于对角线位置。写出Be与氢氧化钠溶液反应的化学方程式:_________________________________。
(3)写出氢,氧,钠,硫四种元素组成的两种酸式盐发生复分解反应的离子方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸是合成治疗禽流感和甲型H1N1流感药物——达菲的重要原料。已知莽草酸的结构简式如图所示。下列关于这种有机化合物的说法正确的是( )

A.莽草酸的分子式为C6H10O5
B.莽草酸能使溴的四氯化碳溶液褪色
C.莽草酸遇FeCl3溶液显紫色
D.1mol莽草酸与足量氢氧化钠反应,最多消耗氢氧化钠4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃时,在容积不变的密闭容器中发生反应X(g)+3Y(g) ![]() 2Z(g),各组分在不同时刻的浓度如表所示,下列说法正确的是( )
2Z(g),各组分在不同时刻的浓度如表所示,下列说法正确的是( )
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 0.1 | 0.2 | 0 |
2 min时浓度/(mol·L-1) | 0.08 | a | b |
平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.1 |
A.平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.平衡后,增大体系压强,v正增大,v逆减小,平衡向正反应方向移动
D.前2 min内,用Y的变化量表示的平均反应速率v(Y)=0.03 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.放热反应都不需要加热就能发生
B.同温同压下,H2 (g) +Cl2(g) =2HCl (g)在光照和点燃条件下放出的能量不同
C.保持其它条件不变,增加反应物的量或增大压强,反应速率就会随之改变
D.使用催化剂会加快反应速率是因为催化剂降低了反应物的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.如图转化关系所示(部分反应物略去):组成单质丁的元素存在三种核素,其中一种核素没有中子。三种核素中质量数最大的原子可表示为__________

(1)由组成单质丁的元素与另一种元素形成的三核 10电子微粒所构成的物质的用途__________________________
(2)乙为 NaOH,若戊为不溶于强酸,但溶于强碱的沉淀物,则甲乙反应时作氧化剂的是__________________
(3)丙→戊反应的化学方程式为_______________________
(4)若戊为既能溶于强酸又能溶于强碱的沉淀物,则甲和乙反应的离子方程式为____________________
II.A、B、C、D 是原子序数依次增大的五种短周期主族元素,其中 A 的原子序数是 B 和 D 原子序数之和的 1/4,C 元素的单质能在A 元素最高价氧化物中燃烧,甲和丙是 D 元素的两种常见氧化物,乙和丁是 B 元素的两种常见同素异形体,1 L 0.005mol·L-1 戊溶液中含 H+ 0.01mol。它们之间的转化关系仍如上图所示(部分反应物省略),
(5)B、C 的元素符号分别是____________________、___________________________其甲和乙反应生成丙和丁的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,错误的是 ( )
A.配制 5%食盐溶液时,称量 5g 食盐放入烧杯中加入 95g 水搅拌溶解
B.胆矾晶体结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.测定未知 NaOH 溶液浓度时,红色手柄滴定管需用标准酸液润洗 2﹣3 次
D.配制 0.1 mol/L 的 H2SO4 溶液时,将量取的浓 H2SO4 放入容量瓶中加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在化学工业中有诸多用途。请回答下列问题:
(1)硼氢化钠NaBH4是硼的重要化合物。
①NaBH4中B元素的化合价为______。
![]() 工业上可利用硼酸甲酯B(OCH3)3与氢化钠NaH反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为______。
工业上可利用硼酸甲酯B(OCH3)3与氢化钠NaH反应制备NaBH4,反应的另一种产物为甲醇钠(CH3ONa),该反应的化学方程式为______。
③NaBH4与水反应生成NaBO2和H2,该反应生成的氧化产物与还原产物的物质的量之比为______。
(2)工业上以铁硼矿![]() 主要成分为Mg2B2O5·H2O和Fe3O4,还有少量
主要成分为Mg2B2O5·H2O和Fe3O4,还有少量![]() 、FeO、CaO、
、FeO、CaO、![]() 和
和![]() 等
等![]() 为原料制备单质B的工艺流程如图所示:
为原料制备单质B的工艺流程如图所示:
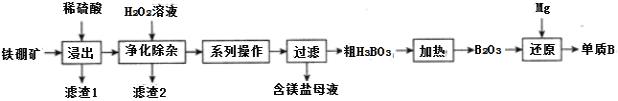
已知:
金属离子 | Fe3+ | Al3+ |
开始沉淀的pH | 2.7 | 3.1 |
沉淀完全的pH | 3.7 | 4.9 |
![]() “浸出”时,将铁硼矿石粉碎的目的为______。
“浸出”时,将铁硼矿石粉碎的目的为______。
![]() 滤渣1的主要成分为______。
滤渣1的主要成分为______。
![]() “净化除杂”时需先加H2O2溶液,其目的为______,然后再调节溶液的pH≈5.0的目的是______。
“净化除杂”时需先加H2O2溶液,其目的为______,然后再调节溶液的pH≈5.0的目的是______。
![]() 制得的粗硼在一定条件下能生成BI3,BI3加热分解可以得到纯净的单质硼。现将
制得的粗硼在一定条件下能生成BI3,BI3加热分解可以得到纯净的单质硼。现将![]() 粗硼制成的BI3完全分解,生成的
粗硼制成的BI3完全分解,生成的![]() 用0.30mol·L-1Na2S2O3溶液滴定
用0.30mol·L-1Na2S2O3溶液滴定![]() 至终点,消耗18.00mL Na2S2O3溶液。盛装Na2S2O3溶液应用______
至终点,消耗18.00mL Na2S2O3溶液。盛装Na2S2O3溶液应用______![]() 填“酸式”或“碱式”
填“酸式”或“碱式”![]() 滴定管,该粗硼样品的纯度为______。
滴定管,该粗硼样品的纯度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )
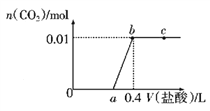
A. a点时溶液中存在c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. 0~a段溶液中水电离出的OH-浓度先增大后减小
C. a=0.2
D. ab段发生反应的离子方程式为CO32-+2H+=H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com